摘要
第四次工业革命推动了以数字化、智能化为特征的健康监测传感器的发展和应用。这些传感器在医疗保健、个人健康管理、老年护理、体育等领域有着广泛的应用,为人们提供更便捷、实时的健康服务。然而,这些传感器面临着诸如噪声和漂移、难以从大量数据中提取有用信息以及缺乏反馈或控制信号等限制。人工智能的发展为数据处理和分析提供了强大的工具和算法,实现了智能健康监测,实现了高精度的预测和决策。通过物联网、人工智能、健康监测传感器的融合,实现实时监测、数据采集、在线分析、诊断、推荐治疗的闭环系统。本文从材料、器件结构、系统集成、应用场景等方面综述了智能技术增强医疗保健人工传感器的研究进展。具体来说,本文首先介绍了可穿戴传感器在监测呼吸频率、心率、脉搏、汗水和眼泪方面的巨大进展;用于心血管护理、神经信号采集和神经递质监测的植入式传感器;用于精确治疗的软性可穿戴电子设备。重点介绍了近年来在挥发性有机物检测方面的研究进展。接下来,对人机界面、人工智能增强的多模传感器和人工智能增强的自我可持续系统的当前发展进行了综述。最后,对今后的研究方向进行了展望。综上所述,人工智能与人工传感器的融合将为下一代医疗保健和生物医学应用提供更加智能、便捷、安全的服务。
介绍
第四次工业革命(工业4.0)的发展推动了以数字化和智能化为特征的健康监测传感器(hms)的快速发展和应用(Shi, Qiongfeng et al. 2020a;Yang et al. 2022c;Zhang et al. 2023)。hms广泛应用于医疗保健、个人健康管理、老年护理、体育等领域,为人们提供更便捷、实时的健康服务(Cho et al. 2020;Zheng et al. 2020)。健康监测传感器经历了漫长的发展。最早用于心脏监测的传感器出现在20世纪50年代,随后被广泛应用于医学领域(Browder 1956)。可穿戴技术的蓬勃发展将健康监测传感器的使用从医院的临床监测转变为家庭的长期护理,例如可穿戴血糖监测仪(Jessica et al. 2020),运动传感器(Dai et al. 2023;高胜等。2021a, 2021b;Zhang等,2022)和呼吸监测仪。进入21世纪,智能手机的出现使监控数据的可视化成为可能,并逐渐应用于智能家居(Shi et al. 2021)、远程医疗(Wang, C. et al. 2021)、智慧城市(Huang et al. 2023;Zheng et al. 2022)等领域,为人们提供更加便捷高效的服务。
尽管在许多方面取得了重大进展,但健康监测传感器仍然面临许多限制(Beardslee et al. 2020;Lee et al. 2021;李鹏等。2021b;Mohankumar et al. 2021)。首先,传感器可能会受到噪声和漂移的影响,这可能会导致它们提供的测量结果出现波动(Dong et al. 2021;董凯等,2020;Takeda et al. 2014)。然后,随着传感器可用性的增加,收集大量数据变得更容易,更具成本效益(Dong and Wang 2021;周和柴2020)。在理解健康监测传感器产生的大量数据并提取有意义的见解方面,出现了一个重大挑战。例如,在医疗保健应用中,可穿戴传感器可用于监测用户的健康和活动水平。这些传感器产生大量的数据,包括心率、血压和运动等因素。此外,还使用多个传感器来监测目标的各个方面(Borchers and Pieler 2010;Dong et al. 2022)。这些传感器可能彼此独立(Poitras et al. 2019),这意味着它们不是为协同工作或提供被监控系统的统一视图而设计的。此外,传统传感器通常具有开环特征,缺乏来自其监测系统的反馈或控制信号(Ellison et al. 2022)。因此,虽然这些传感器可以收集测量或观察结果,但它们无法直接影响系统的行为。这些限制阻碍了传统传感器向更智能和响应能力的发展。
人工智能(AI)的广泛应用是工业4.0的显著特征(Huang et al. 2023)。人工智能的发展历史可以追溯到20世纪50年代(钢2007)。早期的人工智能技术主要依赖于符号逻辑和专家系统。随着时间的推移,人工智能技术经历了多次转型和进步。20世纪80年代,机器学习开始成为人工智能的主要分支,使计算机能够从数据中学习模式,并做出预测和决策(Langley, 1984)。随着计算机技术的飞速发展,特别是云计算和大数据技术的出现,人工智能迎来了新的发展机遇。深度学习成为人工智能领域的主要技术,通过构建多层神经网络,可以处理大量数据,实现高精度的预测和决策(LeCun et al. 2015)。在健康监测传感器领域,人工智能的发展为数据处理和分析提供了强大的工具和算法,为hms面临的开发局限性提供了解决方案(Zhang et al. 2023)。hms收集的数据可以使用AI算法进行处理和分析,从而实现智能健康监测(Gao, S. et al. 2021a)。同时,机器学习算法可以从大数据中挖掘潜在的健康问题,为医生和患者提供更准确的诊断和治疗方案(Wen, F. et al. 2020a, 2020b, 2020c)。将物联网(IoT)技术、人工智能技术和HMS相结合,实现实时监测、数据采集、在线分析、诊疗建议的闭环。此外,通过采用加密、身份认证等技术,保证了健康数据的安全性和患者的隐私性。人工智能在健康监测传感器的发展中起着至关重要的作用。人工智能增强传感器将为医疗保健和生物医学应用提供更智能、更方便、更安全的服务。
本文重点介绍了人工传感器增强的智能技术的发展(图1)。在第2节中,我们介绍了用于监测呼吸频率、身体运动、脉搏、汗水、眼泪等的可穿戴传感器。第3节介绍了能够实现心血管压力检测、神经信号采集和神经递质监测的植入物。第4节介绍了用于治疗的柔性电子器件。在第5部分中,综述了基于光学和电学原理的挥发性有机化合物(VOC)检测传感器以及人工智能增强的VOC平台。在第6节中,提供了人机界面的进展。在第7节“AI增强型多模传感器”中,介绍了结合压力、温度、湿度、无线传输和AI技术的各种多模传感器。在第8节中,提出了一个人工智能增强的自我可持续系统。最后,在第9节中给出了一个简短的结论和观点。
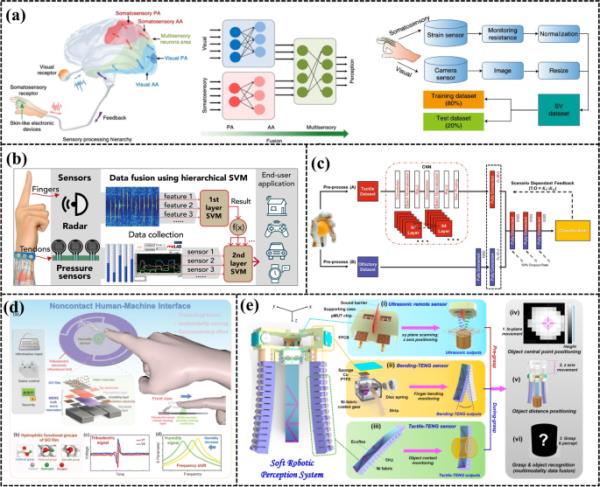
智能技术使人工传感器的发展概况。这张图展示了传感技术(左侧)和人工智能技术(右侧)的发展路线图,以及自供电、可植入、可穿戴传感器和智能家居、机器学习(ML)、VOC传感和人机界面等多种应用的发展
可穿戴式传感器
可穿戴物理传感器
通过增强外部设备功能来提高生活质量的愿望推动了可穿戴电子产品向多功能可穿戴系统的不断发展(Ates等人,2022;他等人。2021;他和李2021;Xu et al. 2019)。目前,商业上可用的可穿戴设备,如腕带、手表和眼镜,通常由佩戴在人体上的刚性元件和柔性腰带组成。然而,为了进一步优化可穿戴舒适性并实现与人类的高级医疗保健互动,可穿戴电子设备现在正朝着具有出色的灵活性,可拉伸性甚至自愈能力的平台发展,受益于功能柔性材料发展的重大进步(Liu等人。2017;Wang and Urban 2020)。与此同时,可穿戴传感器已经进入数字健康领域,在生物医学环境中找到了多种应用。这些传感器可以监测生命体征(呼吸频率、血压、皮肤温度、脉搏等)(迪亚斯和保罗·席尔瓦·库尼亚2018;Iqbal et al. 2021;Wang, C. et al. 2018a),以及生理信号(心电图(ECG)、肌电图(EMG)、脑电图(EEG)等)(Chen et al. 2020;Chi et al. 2010;田磊,等。2019a)。它们还可以捕获身体动力学,如应变和压力(Bai et al. 2022;高珊等。2021a, 2021b;张震等。2020;Zhou, Z. et al. 2020a, 2020b),以及通过可获得的生物体液(如汗液)动态生物分子状态(He et al. 2023;文,冯等。2020a)。
最近,Kim等人开发了一种名为“可调谐、超灵敏、自然启发的表皮传感器”(TUNES)的传感器,它显示出检测范围广泛的信号的能力,从微小的脉冲到更大的肌肉收缩和呼吸(Kim等人,2023)。如图2a所示,作者开发了一种传感器,它模仿了蜘蛛狭缝器官的几何形状和调节机制。通过在金属化聚酰亚胺(PI)薄膜上制造纳米级裂缝,并通过预应变(类似于蜘蛛腿)调整传感器的灵敏度,他们能够使用单个传感器测量不同尺度的应变和压力。事实证明,TUNES可以有效地测量不同脉搏点的脉搏波,甚至可以在步行或骑自行车等体育活动中测量。为了证明TUNES作为非侵入性生物医学传感器的潜力,设计了一个应变可控框架来监测皮肤上的各种生命信号。为了评估传感器的准确性和可靠性,进行了临床试验,将其性能与被广泛认为是血管内血液测量的金标准的压力丝进行了比较。呼吸频率是一项重要的生理参数,可用于识别严重的呼吸系统疾病,如心肺骤停、慢性心力衰竭或肺炎。图2b展示了通过氧化化学气相沉积(oCVD)在面罩上制造的呼吸速率传感器,这是一种独特的方法,可以形成具有可调厚度的图案聚合物薄膜,使传感器保持织物的优势特性(Clevenger et al. 2021)。高导电性聚(3,4-乙烯二氧噻吩)(PEDOT)层成功沉积在一次性手套和口罩上,作为电阻传感器,可实时提取血压信息和呼吸频率,精度很高。该传感器通过测量与佩戴者呼吸相关的电流变化来工作,分别检测电流下降和恢复时的吸入和呼出周期,并测量每个周期电流变化的持续时间和数量。通过分析这些变化,传感器可以估计佩戴者的呼吸频率并识别异常范围,这可能表明各种健康状况,如肺部退化、焦虑、发烧和心脏病。
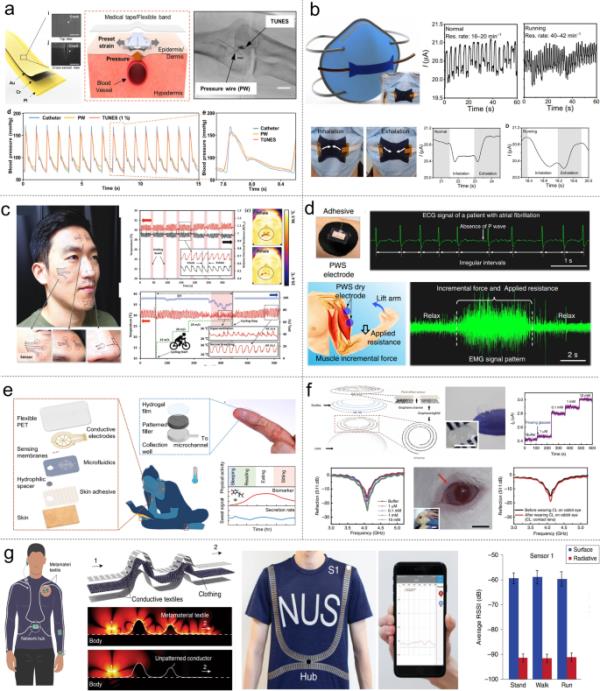
多样化应用的可穿戴技术。a一种可调的、超灵敏的、受自然启发的表皮传感器(TUNES),灵感来自蜘蛛的感觉系统,通过预设应变具有可维持的灵敏度,它不仅可以测量呼吸和肌肉收缩,还可以作为皮肤附着的生物医学传感器(Kim et al. 2023)。b实时检测呼吸模式的呼吸速率传感器,通过将PEDOT沉积在一次性口罩上制成(Clevenger et al. 2021)。c一种敏感而灵活的人造皮肤,包括一个负温度系数热敏电阻,可以贴合在面部皮肤上,从而记录呼出的温度变化(Shin et al. 2020)。d一种高导电性聚合物干电极(PWS膜),具有优异的导电性、可拉伸性和自粘附性,可在不同条件下实现高质量的ECG、EMG和EEG信号采集(Zhang, L. et al. 2020)。e一种可穿戴贴片,可在休息期间连续监测热调节性汗液的组成和速率,该贴片采用快速吸汗机制,最大限度地减少汗液积累所需的时间,从而实现实时测量(Nyein等人,2021)。f一种用于无线眼部诊断的多功能隐形眼镜传感器,可检测泪液中的葡萄糖和眼压(Kim et al. 2017)。g互联无线身体传感器网络,以能源效率和增强的安全性为特征,利用无线电表面等离子体在超材料纺织品上传播(Tian, X. et al. 2019b)
温度传感在提供各种科学和工程领域的关键数据方面发挥着关键作用。最近,由于在人工皮肤和连续生理温度跟踪等应用中需要灵活灵敏的温度监测,人们对可穿戴温度传感器的兴趣日益浓厚。图2c展示了一种制造具有负温度系数(NTC)热敏电阻的高灵敏度和柔性人造皮肤的新方法,这是通过独特的无缝结构和单片激光诱导还原烧结方法实现的(Shin et al. 2020)。利用热敏聚合物基板,可以制造具有更高温度敏感性的电子皮肤。氧化镍(NiO)温度传感器可以与面部表面的各种曲率一致地连接在一起,从而可以长时间连续准确地测量生理温度。已经证明,它可以捕捉到与吸入和呼出有关的微小温度变化。此外,它还能够准确监测剧烈体育活动期间呼吸模式的变化。结果显示,当血氧饱和度较低时,呼吸频率显著上升27%,温度变化幅度显著降低65%,表明呼吸浅。这些发现突出了它作为一种非侵入性生理监测系统的潜力,特别是对于经历代谢或病理性失衡状况的危重患者。
准确记录人体生物电位信号对于诊断和治疗心脏、大脑和肌肉相关疾病至关重要,这依赖于使用与皮肤有效连接的高效可穿戴电极。如图2d所示,Zhang等人开发了一种高导电性的聚合物干电极(PWS膜),具有显著的自粘性、可拉伸性和导电性等特性(Zhang, L. et al. 2020)。它是通过由PEDOT: PSS,水性聚氨酯(WPU)和d -山梨醇组成的混合物的溶液处理实现的。在静态和动态测量中,PWS薄膜在较低的皮肤接触阻抗和噪声水平方面优于传统的干电极和凝胶电极。因此,它可以在不同条件下采集高质量的ECG、EMG和EEG信号。为了评价PWS干电极的疗效,我们进行了一项临床研究。本研究包括心电图心律失常的识别,深肌腱反射测试中肌肉活动的检测,以及收缩和放松时肌肉力量的量化。心电图结果显示与心房颤动一致的异常模式,而PWS干电极获得的肌电图信号准确地捕获了各种任务期间肌肉活动的变化。这些发现突出了PWS干电极在临床评估与心脏和肌肉功能相关的神经系统疾病方面的潜力。
可穿戴化学传感器
对个人健康状况的全面评估需要收集广泛的信息,包括来自人体或其附近的生命体征、身体活动和化学生物标志物。为了满足这一需求,可穿戴化学传感器已经被开发出来,用于实时检测生物流体和周围环境中的生物标志物(He et al. 2023;文,冯等。2020a)。这些传感器利用不同的转导机制,可以检测生物流体(如眼泪或汗液)中出现的各种生物标志物,这可能会增强疾病的预测、筛查、诊断和治疗。图2e显示了最近的一项研究,该研究展示了一种可穿戴贴片,旨在连续跟踪休息期间的出汗率(Nyein等人,2021)。为了解决休息时低汗液分泌率的挑战,微流体集成到贴片中,可以防止蒸发并选择性地检测汗液率。此外,层压亲水性填料被纳入,使汗液快速吸收到传感通道,从而减少汗液积累时间。该贴片在微通道中具有功能化的电化学电极和电电极,可同时检测pH、Cl-1、左旋多巴和出汗率。由于体积小巧,该装置已被有效地用于测量手指、肩膀、胸部等身体不同部位休息时的汗液分泌率。该贴片已经过测试,以评估其在轻度体育活动、血糖波动和帕金森病药物管理期间的动态出汗行为的性能,证明其作为临床和研究环境中个人生理状态和医疗状况日常监测的理想平台的潜力。在无创健康监测方面,眼泪和唾液比汗水有几个优势。这些体液积累时间短,体积足够,无需额外的提取方法。由于其生物相容性和顺应性,隐形眼镜作为一种可行的撕裂传感器基底引起了人们的极大关注。然而,为了解决与眼球接触的电线引起的潜在炎症风险,有必要在基于隐形眼镜的泪液传感器和测量设备之间建立无线连接。例如,如图2f所示,Kim等人介绍了一种使用石墨烯场效应晶体管(FET)和石墨烯-银纳米线(AgNW)复合天线集成的撕裂传感器,该传感器在射频下工作,并在石墨烯通道上发生葡萄糖氧化时无线传输传感信息(Kim等人,2017)。它专门用于检测泪液中的葡萄糖水平,并利用电阻和电容特性测量眼压。本文成功地实现了兔眼泪液中葡萄糖的实时检测和牛眼球中眼压的无线跟踪。
可穿戴身体传感器网络
传感器、智能设备和显示器在人体内的集成是可穿戴电子研究的一个重要发展。然而,为这些设备建立一个功能网络带来了挑战,例如传感器节点之间的直接连接导致的物理活动中断。尽管可穿戴电子产品在将传感器和电线集成到服装或皮肤上方面取得了进展,但将它们与其他提供电力和收集数据的功能部件连接起来仍然具有挑战性。因此,无线互连方法对于创建离散可穿戴设备网络至关重要,在保持可用性和用户舒适度的同时,实现无缝通信和功能。无线技术,包括蓝牙和Wi-Fi等基于无线电的方法,通常用于连接可穿戴传感器,用于健康监测和临床通知。然而,这些技术需要为每个传感器节点提供离散的电源,面临着皮肤一致性有限、隐私问题和定期更换电池的问题。近场通信(NFC)提供了一种替代方法,传感器可以通过读取器无线供电,实现无电池和安全的操作,用于皮肤或体内的各种生理测量(Lin等人,2020;Lin et al. 2022;Niu et al. 2019;Shi et al. 2022)。图2g展示了一种利用超材料纺织品构建纺织品可穿戴传感系统的创新技术,该技术可使无线电表面等离子体在人体表面传播,从而实现安全、节能的无线人体传感器网络(Tian, X. et al. 2019b)。该方法在服装中使用导电织物,在无线电通信频率上促进表面等离子体模式,从而使人体传感器网络的传输效率明显高于没有超材料纺织品的传统辐射网络。此外,无线通信被限制在距离身体10厘米的范围内,确保传感信号是安全的,不会被周围区域的外部来源拦截。一个由两个传感器节点(蓝牙模块在肩膀和下背部)和一个智能手机中心组成的网络安装在腹部,以展示节能通信。在一组健康志愿者进行体育活动时,对信号强度进行了实时检测,结果显示,与对照组相比,这两种设备的信号强度增强了31 dB。信号传输效率提高了1000倍,从而降低了功耗,提高了数据传输速度。这些发现表明,衣服可以用来操纵身体周围的电磁波,为将微波或光子电路的概念集成到纺织品中提供了基础,并使无线传感、信号处理和能量传输应用成为可能。
体内健康监测
与监测体表汗液标志物的可穿戴传感器(Gai et al. 2022)、表皮电信号(肌电图、心电、脉搏)(Liu et al. 2022a、2022b、2022c、2022d、2022e;欧阳等,2017)和肢体动作再通化(Wang, C.等,2020a, 2022b, 2020c;Wang, C. et al. 2021)等,植入式传感器在体内功能更直接地执行健康状态。例如,心脏和血管的正常功能(Ouyang et al. 2021),损伤组织的恢复进展(Zhang et al. 2021),中枢神经信号的异常(Shin et al. 2021)等,都需要在体内植入设备进行长期状态监测(Jiang et al. 2020)。同时,植入式器件的研究对材料选择、结构设计、系统集成、供电、生物安全等方面也提出了很高的要求(Jiang et al. 2018;Wang et al. 2019;Yao et al. 2022;Zhao et al. 2019)。
体内自供电传感器
近年来,自供电可植入传感器的发展显示出革命性的潜力,通过提供连续和准确的数据,而无需外部电源或频繁更换(Xiao et al. 2022;Yao et al. 2022;Zheng et al. 2020)。Li等人报道了首个基于摩擦电纳米发电机(TENG)原理的自供电植入式生物电子学(SIBE) (Zheng et al. 2014)。之后,凭借重量轻、成本低、输出能量密度高的优势,SIBE在体内能量采集、心血管监测、心脏起搏、肌肉/神经电刺激、组织再生、药物输送等领域脱颖而出。根据世界卫生组织(WHO)的统计数据,全球每年约有1790万人死于心血管疾病,占全球死亡人数的31%。心血管疾病也是导致残疾的主要原因之一(Ouyang et al. 2019;石毅等,2020c;Wang et al. 2022)。Ma等人开发了一种可植入的主动压力传感器,名为iTEAS,用于实时生物医学监测,如图3a所示(Ma et al. 2016)。基于摩擦电效应原理,itas能够将植入部位运动产生的机械信号转换为可读电信号,进一步分析心率、血压、血流量和呼吸频率(图3ai)。同时,iTEAS可以从人体中获取机械能,并将其转化为电能进行自我供应,克服了电池容量的限制(图3aii)。经过良好的包装后,这种主动传感器在胸腔闭合后72小时内仍保持监测功能,并表现出良好的生物相容性(图3aiii)。图3b, (Liu et al. 2019)提出了一种使用与微创植入心脏导管集成的自供电压力传感器(SEPS)监测心内压的新方法。经优化探索,SEPS的灵敏度为1.195 mV/mmHg,线性关系R2=0.997。SEPS通过体外和体内实验证明了其可行性,通过提供微创和自供电的解决方案,解决了传统侵入性监测方法的局限性。
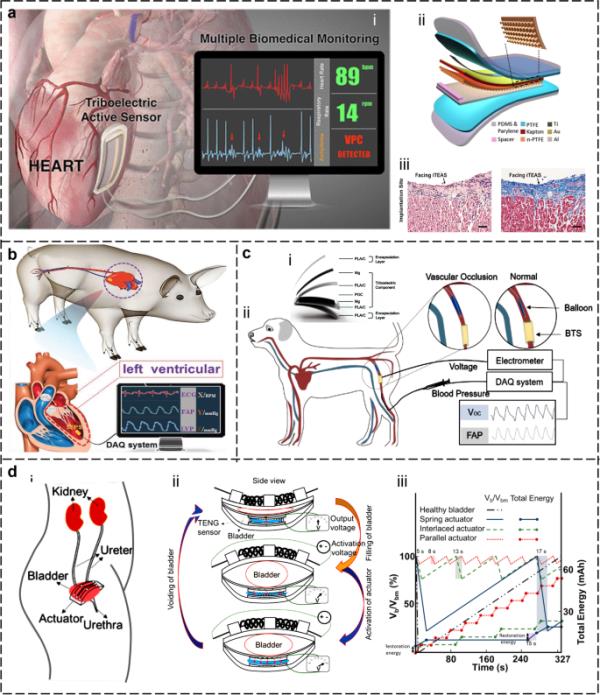
用于体内医疗保健的自供电传感器。a一种多功能摩擦电主动传感器,用于精确、连续和实时监测多种生理和病理体征(Ma et al. 2016)。b用于心内压监测的小型化、柔性压力传感器,可与微创导管结合使用(Liu et al. 2019)。c一种可降解和可吸收的主动压力传感器,用于血压监测和异常心血管事件的诊断(Ouyang et al. 2021)。d一种基于形状记忆合金的自我控制系统,用于神经源性活动不足膀胱的压力监测和自主排尿控制(Arab Hassani et al. 2018)
瞬态电子在完成其服务后可以在体内降解和吸收,从而使患者免于疼痛和第二次手术移除植入物的感染风险(Chao et al. 2020;Li et al. 2018;Li et al. 2023;郑强等,2016)。欧阳等人描述了用于心血管术后护理的生物可吸收摩擦电传感器(BTS)的发展(图3c)(欧阳等人,2021)。基于摩擦电效应,BTS被设计为植入体内,能够实时监测压力变化。BTS有可能通过提供准确和连续的压力监测来改善患者的预后,而没有与永久植入物相关的风险。人的泌尿系统是由神经和肌肉系统的协调作用来调节的。这些系统的任何异常都可能导致严重影响日常生活的泌尿系统疾病。图3d,介绍了监测膀胱压力和控制排尿的控制系统(Arab Hassani et al. 2018)。在该系统中,使用基于teng的压力传感器来检测膀胱的填充状态。采用一种基于形状记忆合金的双稳态微致动器来诱导膀胱收缩和舒张排尿。这是一个很好的尝试,为今后的临床应用提供了可靠的途径。总的来说,这些研究证明了自供电、可植入传感器的潜力,将彻底改变生物医学监测领域。这些传感器可以实现各种参数的准确和连续监测,而无需频繁更换或外部电源。随着技术的不断发展,自供电植入式传感器有望成为医疗保健领域越来越重要的工具,特别是在心脏病学、神经学和术后护理领域。尽管已经取得了重大进展,但在新材料、多模态集成和更有效的组织-设备接口领域仍有改进的空间(Wen et al. 2023)。例如,具有组织粘附特性的胶粘剂水凝胶的开发可以无缝地将植入物固定在生物组织表面,增强界面相互作用,同时避免手术缝合对组织表面造成的损伤(Wang et al. 2023)。人体是一个复杂的系统,对人体健康状态的监测需要多个功能装置协同工作,对系统集成和信息处理提出了新的要求。
神经接口
神经系统是人体的控制中心,调节器官活动和调节对外界刺激的反应。监测神经电信号或神经递质可以洞察生理和病理过程,为神经系统疾病的预防和治疗提供信息(Cho et al. 2020;Lee, S. et al. 2017;Lee et al. 2022)。然而,由于神经信号强度弱、噪声高的特点,准确获取和解读神经信号并不容易(Cho et al. 2020;Xiang et al. 2016a)。此外,神经电极与神经组织的适形匹配也是影响神经界面(NIs)稳定性和生物相容性的关键因素(Liu, Y. et al., 2020;Song et al. 2020)。各种NIs如电极阵列、场效应管、微/纳米机械系统(MEMS)和纳米通道阵列用于测量神经信号(Lee, Sanghoon等人,2017)。同时,微电极阵列、纳米通道阵列和光学生物传感器通常用于检测神经递质浓度(Song et al. 2020;Wang, J.等人,2018)。提高神经网络与神经组织的适应性和功能的长期稳定性;提高神经电极的高空间分辨率和开发可与其他神经技术集成的神经电极一直是该领域的研究重点。图4a介绍了一种柔性且具有生物相容性的神经带状电极(NRE),通过缠绕神经纤维实现了对各种直径神经的自适应(Xiang et al. 2016b)。NRE表面涂有电稳定性的碳纳米管,这确保了与神经组织的密切三维非侵入性接触和稳定的通信。大鼠体内实验表明,NRE可以无创地记录腓神经、胫神经、腓肠肌神经等小神经的神经信号,这是传统袖带电极无法实现的。凭借这些独特的功能,神经带电极有可能通过与精细神经密切相关的器官交流来特异性控制目标器官,并将有助于建立高灵敏度,实时和精确的反馈,以了解未知的电化学机制。与表面电位信号相比,神经纤维束内部信号包含更多与肢体运动和感觉功能恢复相关的传导和反应。图4b展示了一种新型刺状超柔性神经界面(SUNI),它通过刺状结构从大鼠机械感受器收集感觉信息(Wang, J. et al., 2018)。SUNI新颖的三维结构设计使其与神经纤维束的适形接触良好。SUNI的高质量记录有助于区分触觉和本体感觉刺激,并进一步提供高空间分辨率的神经信号分类。
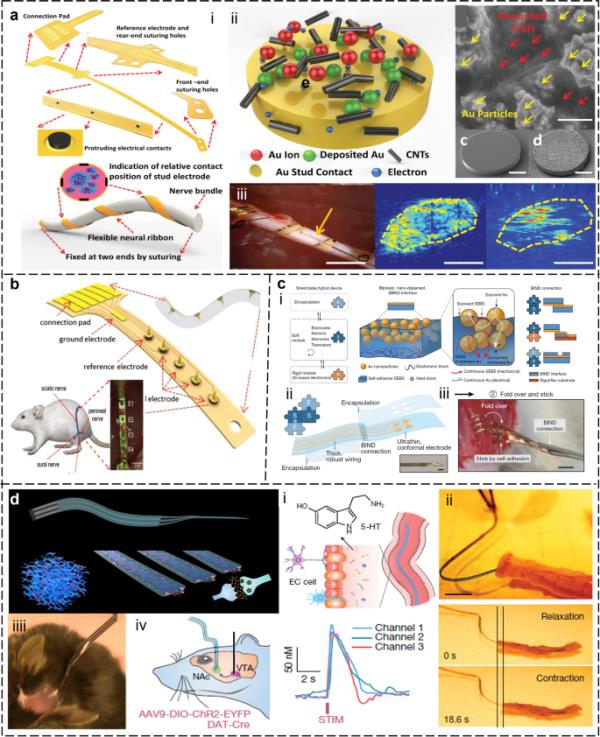
基于柔性神经接口的神经信号传感。a用于记录周围小神经信号的自适应、无创一般神经带状电极。i:神经带状电极(NRE);ii:神经电极三维接触点;iii: NRE的体内性能(Xiang et al. 2016b)。b具有3D尖峰结构的柔性神经电极可以精确监测和解码周围神经信号,以恢复运动感知(Wang, J. et al. 2018b)。c基于双相分散金纳米颗粒的通用接口,可以以即插即用的方式连接柔性/刚性模块。i - ii:柔性模量与刚性模量的积分方式示意图;iii:将BIND电极作为电极应用于腓骨长肌(Jiang et al. 2023)。d用于大脑和肠道的柔软可拉伸的基于石墨烯的生物传感神经接口。i - ii:肠内用于化学感应的神经串;iii - iv:用于脑神经信号记录的NeuroString (Li et al. 2022)
硬的疏水NIs与软的湿的神经组织不匹配是导致免疫排斥和神经电极失效的最重要原因。针对这一问题,研究热点主要集中在三个方面。首先,设计具有柔性链接结构的本质硬微硅基器件,如岛桥结构、s形结构、波浪结构等,赋予植入物在小范围内弯曲和拉伸的能力(Song et al. 2020)。其次,使用柔性材料作为植入物与生物组织之间的桥梁(Liu, Y. et al. 2020b)。Zhao等人报道了几个设计柔性和粘性水凝胶作为手术器械涂层的例子(Yu et al. 2019)。第三,开发基于先进软质材料的内在可拉伸植入物。图4c展示了一种巧妙的方法,将刚性模块和软模块之间的一站式通用界面(UI)组合在一起(Jiang et al. 2023)。该UI以即插即用的方式可靠地连接软、刚性和封装模块,形成坚固且高度可拉伸的电子设备。UI由互穿聚合物和金属纳米结构组成,通过简单的压制连接模块,而不使用粘合剂。软、软、硬模块之间的连接均表现出良好的机械和电气拉伸性。此外,与该接口组装的电子设备用于体内神经调节和皮肤肌电图监测,具有高信号质量和机械稳健性。这些即插即用的接口简化并加速了皮肤和植入式可伸缩电子产品的发展。对于柔软和可拉伸的植入物,Liu等人报道了一种变形植入式电子(MIE),它以最小的机械约束适应神经组织的生长(Liu, Y. et al. 2020b)。MIE由可拉伸应变传感器和以可拉伸聚二甲基硅氧烷-异佛尔酮双脲(PDMS-IU)为包被层、导电聚合物PEDOT: PSS为导电层的神经电极组成,在监测组织生长的同时提供电刺激。在大鼠生长最快的时期,变形电子设备对大鼠神经的损伤最小,其直径增长了2.4倍。MIE展示了神经接口柔性和可拉伸电子器件的独特优势。图4d给出了同一研究小组的另一个例子(Li et al. 2022)。研究人员展示了一种类似组织的可拉伸传感器,名为NeutroString,用于监测单胺类神经递质。NeuroString通过将Fe3O4或NiO纳米颗粒加载到激光诱导PEI形成的石墨烯上,实现了对不同神经递质的电化学检测,解决了单层石墨烯的弱应变限制。同时,采用生物相容性聚苯乙烯-嵌段聚乙炔-丁烯-嵌段聚苯乙烯(SEBS)作为柔性衬底和封装层,实现了类组织的柔性和力学模量。NeutroString能够与大脑和肠道组织无缝对接,在不干扰实验动物正常行为的情况下实现对神经递质的长期监测。
总之,植入式神经接口近年来取得了重大进展,为理解和连接神经系统提供了新的机会(Cho et al. 2020;Lee, Sanghoon et al. 2017;Xiang et al. 2016a)。这些神经接口被设计成与神经组织相互作用,允许记录和刺激神经活动,并有望治疗神经疾病和恢复失去的功能。尽管如此,作为一种临床工具,仍有重大挑战需要解决。主要挑战之一是开发能够承受恶劣生物环境并避免对周围组织造成损害的长期稳定界面(Song et al. 2020)。另一个挑战是需要提高神经记录和刺激的分辨率和特异性,以及与大量神经元交互的能力(Li et al. 2022)。此外,为这些装置的植入和监测制定安全有效的临床方案,以及监管和伦理考虑,是未来研究和发展的重要领域。总的来说,植入式神经接口的进展是有希望的,该领域的持续研究和发展将为理解和治疗神经系统疾病提供新的机会。
灵活的电nic用于治疗
可穿戴技术的最新进展通过实现以前不可能的创新治疗方法,彻底改变了医疗保健。随着柔性电子产品的引入,智能可穿戴医疗设备(iwmd)的发展已经成为现实,促进了各种医疗状况的实时监测、诊断和治疗(Tan et al. 2022)。这些设备在寻求个性化医疗保健和克服被动治疗的局限性方面取得了巨大的重要性。通过追踪生理和病理因素并按需提供治疗药物,大规模杀伤性武器在提供预测性生物分析、及时治疗干预和提高药物疗效方面已成为不可或缺的,从而促进了精准医疗(cheol Jeong et al. 2018;Tan et al. 2022)。
由于其灵活性和可扩展性,用于透皮/局部给药的可穿戴给药设备比口服和注射等传统方法更受欢迎。这些装置已被用于连续和响应性地递送一系列治疗剂,包括多肽、多糖、小分子和生长因子(Kar et al. 2022;杨媛等。2022a;杨,袁等。2022b)。例如,a . Tamayol的团队开发了一种可穿戴和可编程的绷带,它结合了聚合物微型针阵列(MNAs),以促进必需药剂和生长因子的靶向递送到伤口的更深层(图5a) (Derakhshandeh et al. 2020)。这种绷带具有独特的能力,可以通过MNAs主动递送具有独立时间谱的多种药物。血管内皮生长因子(vascular endothelial growth factor, VEGF)作为一种治疗药物,不仅要选择合适的治疗方法,而且要考虑其在伤口床内的输送技术和空间分布。在使用可编程平台对糖尿病小鼠慢性皮肤伤口施用VEGF的情况下,与传统的局部应用治疗方法相比,在伤口愈合、再上皮化、血管生成和毛发生长方面观察到显著的增强。图5b展示了一种新的方法,通过利用装载PS和O2推进剂的微针(MN)贴片,以更深、更快的方式实现光敏剂的透皮递送,并改善光动力治疗(PDT) (Liu, P. et al. 2022b)。为了提高PDT性能,将过碳酸钠(SPC)加入到溶解聚乙烯基吡罗烷酮微针中。SPC在微针中的包含导致了一种独特的机制,它与周围的流体反应,产生气态氧气气泡。这些气泡诱导了剧烈的流体流动,导致氯e6 (Ce6)在水凝胶模型和皮肤组织中的渗透性显著增强。为了评估这种气态氧驱动递送PS的有效性,在荷瘤小鼠模型上进行了20天的治疗。结果显示肿瘤生长速度降低,肿瘤体积减小,证实了采用该方法时PDT的疗效提高。
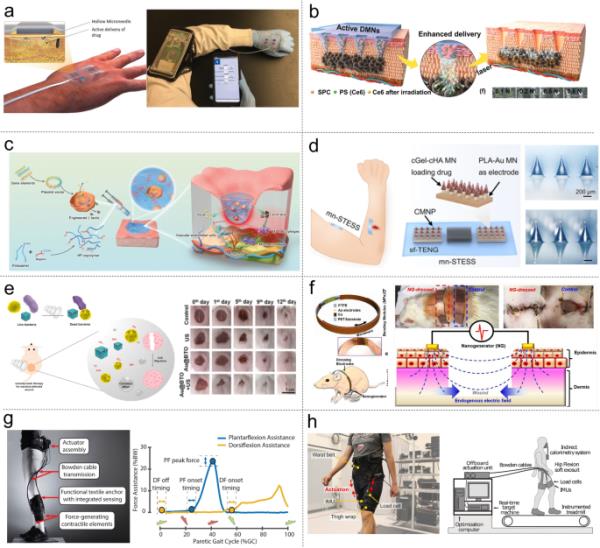
用于伤口愈合、药物输送和康复的可穿戴电子设备。a一种可穿戴和可编程的绷带,能够将必需的药物化合物和生长因子输送到伤口部位的更深区域(Derakhshandeh et al. 2020)。b一种含有PS和O2推进剂的微针贴片,使PS的透皮递送更有效,并增强光动力治疗的有效性。(Liu, P. et . 2022b)。c工程细菌激活热反应水凝胶促进糖尿病伤口愈合(Lu et al. 2021)。d利用微针的自我维持经皮电刺激系统增强表皮生长因子的药效学(Yang, Yuan et al. 2022d)。e一种新型声敏剂Au@BTO,将金纳米颗粒与改进的肖特基结结合到压电纳米复合材料(BTO)中,用于高效的声动力治疗(Wu et al. 2021)。f通过电刺激促进皮肤伤口愈合的电绷带(Long et al. 2018)。g一种利用软机器人技术的辅助康复服,用于从中风相关的行走障碍中康复的个人。(Awad et al. 2020)。h具有优化髋部屈曲辅助的轻质柔软外骨骼,可减少行走时的能量消耗(Kim et al. 2022)
图5c显示了一个由活乳球菌结合在肝素-波洛沙姆热响应水凝胶中的递送系统。它旨在设计伤口微环境,以动态和时间的方式促进血管生成。利用生命系统,实现血管内皮生长因子(vascular endothelial growth factor, VEGF)的产生和保护,促进内皮细胞的增殖、迁移和成管。此外,该系统分泌乳酸,有助于将巨噬细胞转变为抗炎表型,促进糖尿病伤口的血管生成。重要的是,由于其将细菌种群限制在伤口上的能力,该输送系统可以大大降低全身毒性的风险。因此,该系统具有高效的治疗递送潜力,促进伤口微环境的快速愈合,并有望作为再生医学应用的支架(Lu et al. 2021)。最近,Yang等人开发了一种基于微针的自供电经皮电刺激系统(mn- ess),该系统利用微针集成滑动TENG来增强表皮生长因子的药效学,如图5d所示(Yang, Yuan et al. 2022d)。mn- ess的主要目的是通过微针刺入角质层,提高药物的穿透和利用。此外,它利用手指滑动产生的机械能来发电,通过微针实现经皮电刺激。这种电刺激作为一种补充因子,抵消了谷胱甘肽引起的表皮生长因子的下降,增强了其受体在角质形成细胞中的表达,有效地解决了受体脱敏问题。
声动力疗法是一种高度精确和微创的治疗癌症和消除病原体的方法,这需要高度有效和生物相容性的声敏剂。在最近的一项研究中,Wu等人介绍了一种用于高效声动力治疗的新型声敏剂,它是一种名为钛酸钡(BaTiO3, BTO)纳米立方体的压电纳米复合材料,使用金纳米颗粒修饰肖特基结(Au@BTO),如图5e所示(Wu et al. 2021)。利用超声波作为外部机械波,触发Au@BTO的压电效应,导致压电材料与金属界面处载流子的分离和移动增强。这一过程通过氧化还原反应显著促进了活性氧(ROS)的产生。Au@BTO所展示的ROS生产的特殊效率使其在对抗革兰氏阴性和革兰氏阳性细菌方面都非常有效。此外,体外和体内实验均表明,声动力处理还能促进成纤维细胞的迁移,从而有助于小鼠皮肤伤口的愈合。人们普遍认为,电刺激已被证明是促进皮肤伤口愈合过程的另一种有效方法。图5f描述了一种旨在加速皮肤伤口愈合的电绷带,它通过可穿戴TENG产生交替的离散电场,将身体运动产生的生物机械能转化为电能(Long et al. 2018)。大鼠研究表明,这种方法可以在3天内迅速愈合全层矩形皮肤伤口,明显快于基于收缩的愈合过程。体外研究表明,电场刺激成纤维细胞的迁移、增殖和反式分化,从而加速皮肤伤口愈合。
除了使用生物电子学进行治疗外,还有机器人外骨骼可以通过集成传感、控制和计算机科学直接协助或增强人类活动(Yang et al. 2008)。近年来,专门为下肢设计的外骨骼的开发取得了重大进展。这些外骨骼旨在将扭矩应用于生物关节,帮助行走能力受损的个体或增强健康个体的能力。(Ding et al. 2018;Huo et al. 2014;Lee, G. et al. 2017;Quinlivan et al. 2017)。这些外骨骼系统是典型的机器人机构,由刚性链接、关节和驱动器组成,与下肢平行排列,提供步态训练或康复。C. Wash教授和他的团队致力于开发专门为步态康复设计的外骨骼,并有效地展示了一系列原型,这些原型能够帮助行动不便的个人或通过降低代谢率来增强健康个体的能力。他们最近的外骨骼原型的一个例子如图5g所示,它集成了Bowden电缆、功能性纺织锚、致动器和产生力的收缩元件(Awad et al. 2020)。通过将鲍登电缆连接到鞋垫,辅助力有效地传递到脚踝。将跖屈肌和背屈肌结合在柔软的外服中,在提高中风后患者的行走速度和距离方面显示出有希望的结果。此外,适当设计的外服有可能减少与健康个体行走相关的能量消耗。在图5小时中,研究人员开发了一种柔软轻便的外服,以研究与髋部弯曲支撑相关的生理和生物力学效应(Kim et al. 2022)。通过采用人在环优化,研究人员发现,与现有的最先进的外骨骼相比,这种外骨骼可以显着减少与行走相关的能量消耗,使机械功率降低近50%。研究结果表明,与无辅助行走相比,专门设计用于辅助髋关节屈曲的系留外骨骼服可以有效降低步行时的代谢率约15.2±2.6%。与不穿外套走路相比,这种减少相当于代谢率降低了14.8%。为了帮助肢体受损的人,假肢被设计用来替换缺失或截肢的身体部位,让使用者重新获得功能活动能力并执行日常任务。这些设备通常是定制的,以密切配合用户的解剖结构,并可以通过各种机制进行控制,如肌肉信号或感官反馈。随着技术的不断进步,这些辅助设备预计将变得更加复杂、可定制,并与人体无缝集成,最终使个人能够克服身体限制,实现更大的独立性(Valle等人,2021;Jean Won Kwak等。2020;庄等人,2019)。
目录
摘要 介绍 可穿戴式传感器 挥发性有机化合物的检测 人机接口 人工智能增强的多模传感器 人工智能增强的自我可持续系统 结论 数据和材料的可用性 缩写 参考 致谢 作者信息 道德声明 相关的内容 搜索 导航 #####挥发性有机化合物的检测
光学VOC气体识别
挥发性有机化合物(VOCs)是从各种来源释放的气体,如化学品、清洁剂、建筑材料和人体(Galstyan等人,2021;Lim et al. 2021)。使用呼吸中的挥发性有机化合物气体作为诊断工具是一个有前途的研究领域。有证据表明,呼吸中挥发性有机化合物气体的水平和类型的变化可以表明各种疾病和状况,如图6a所示(Binson和Subramoniam 2022;2018年威尔逊)。例如,一些研究表明,呼吸中的VOC气体可以作为肺癌早期检测的生物标志物(Hakim et al. 2012)。特定的挥发性有机化合物,如苯、甲苯和乙苯,在肺癌患者的呼吸中会升高(Jalal et al. 2018)。某些挥发性有机化合物(如乙烷和戊烷)水平的变化与哮喘有关(Peel et al. 2020)。这些挥发性有机化合物被认为是由气道中的氧化应激产生的,在哮喘发作期间,它们的水平会增加。呼吸中的挥发性有机化合物也可用作检测和监测糖尿病的生物标志物(Behera et al. 2019)。某些挥发性有机化合物(如丙酮和异戊二烯)水平的变化与糖尿病及其并发症有关。
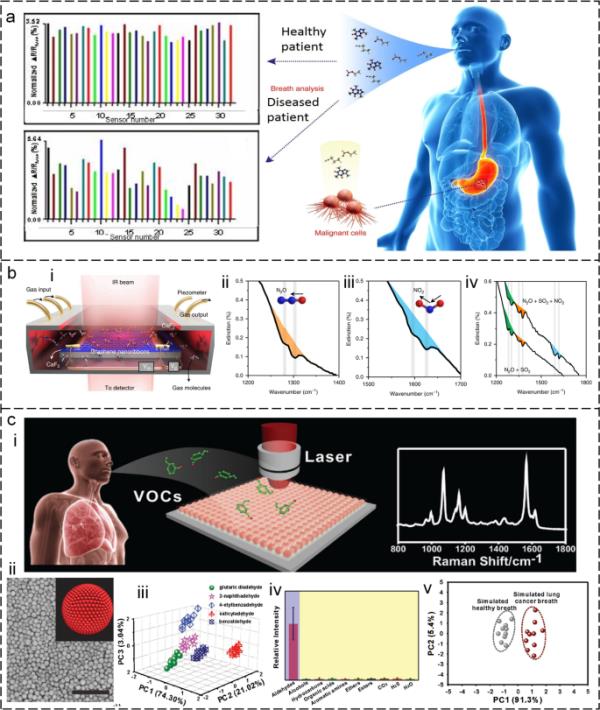
用于医疗诊断的光学挥发性有机化合物(VOC)气体识别。呼吸中的挥发性有机化合物成分用于疾病诊断(Wilson 2018)。b使用基于表面增强红外吸收(SEIRA)效应的传感器识别VOC气体(Hu et al. 2019)。i:示意图。ii-iv:不同氮氧化物的鉴定。c基于表面增强拉曼光谱(SERS)传感器的VOC气体检测。i: SERS平台的概念。ii: SERS平台的SEM图像。iii: 5种VOC气体的检测演示。iv: SERS平台的选择性。v:一组模拟健康和肺癌呼吸样本的PCA (Qiao et al. 2018)
在呼吸中使用挥发性有机化合物气体进行疾病诊断的挑战之一是呼吸样本本身的复杂性和可变性(Yan和Zhou 2022)。呼出气体的成分可能受到各种因素的影响,如饮食、年龄、吸烟状况和药物使用,这可能使识别疾病特异性VOC特征变得困难(Binson和Subramoniam 2022)。此外,呼气中挥发性有机化合物的检测和测量可能具有挑战性,因为许多这些化合物的浓度很低,存在干扰化合物,并且需要灵敏和准确的检测方法。开发超灵敏、选择性VOC气体传感器是应对这些挑战的关键。有许多方法可用于检测挥发性有机化合物,包括电气和光学传感器(Khatib和Haick 2022)。评估VOC气体传感器的关键因素包括:1)灵敏度:指其检测空气中低浓度VOC的能力。高灵敏度对于检测可能指示疾病的微量挥发性有机化合物非常重要(Wang, J.X.等,2020b);2)选择性:选择性是指VOC气体传感器区分不同类型VOCs的能力。这一点很重要,因为不同的挥发性有机化合物会产生不同的健康影响和环境影响(Miah et al. 2022);3)响应时间:VOC气体传感器的响应时间是指传感器检测到空气中VOC浓度变化所需要的时间。快速的响应时间对VOCs的实时监测至关重要;4)稳定性和可重复性:VOC气体传感器的稳定性和可重复性是指其随时间提供一致和准确读数的能力(Liu and Zhang 2021)。
红外(IR)光谱检测VOC具有优势(Lin and Xu 2020;Liu et al. 2021;刘鑫等。2022d;周杰等。2008;Zhu et al. 2021)。因为它不仅可以检测VOC的含量,还可以识别其类型,这对疾病的诊断非常重要。然而,由于该方法的分子吸收截面较低(中红外每分子10-20 cm2),因此检测性能受到限制。红外等离子体纳米天线是一种人工结构材料,经设计可在纳米级运行(Hui et al. 2021;李东晓等。2021a;Xie et al. 2023;徐生等。2022;Zhou et al. 2018;周海等。20119a, 20119b)。这项技术能够通过激发局部表面等离子体的过程,在极高的水平上操纵光,从而产生超强的近场(Xu, C. et al. 2022;周辉等。2020a;周辉等。2022a, 2022b)。通过将VOC分子捕获在纳米天线的近场中,这些分子的红外吸收可以通过一种称为表面增强红外吸收(SEIRA)的现象被放大(Liu, W. et al. 2022c;Ren et al. 2021;Xu et al. 2020)。这是特别有用的,因为VOC分子通常具有低红外吸收截面。Hu等人在2019年展示了这种方法的一个值得注意的例子,他们使用石墨烯纳米带来激发表面等离子体并检测多voc气体的振动,如图6b所示(Hu等人,2019)。气体吸附的机理涉及气体分子通过图像引力和缺陷吸附在石墨烯层上的吸附和积累。检测信号对应于石墨烯表面吸附了一层浓度为800 zeptomoles / μm2的气体分子。该研究成功地检测了几种气体,包括SO2、NO2、N2O和NO,响应时间为1分钟。未来的研究应着重于提高石墨烯的晶体质量和迁移率,从而提高石墨烯等离子体的质量因子和场增强效果。
表面增强拉曼散射(SERS)是一种有效的分析方法,它利用金属纳米颗粒增强电磁场,从而放大VOC分子的拉曼散射信号(Lee etal . 2019;Wong et al. 2014)。气体选择性捕获材料由于其优点,在基于sers的VOC气体检测中至关重要(Ly等人,2021;Song et al. 2021)。首先,这些材料增强了目标气体分子的浓度,从而提高了SERS测量的信噪比。捕获材料允许气体分子集中在小体积内,从而提高了与sers活性金属纳米颗粒相互作用的可能性。此外,捕获材料为SERS测量提供了稳定的环境,防止目标气体分子从检测区域扩散出去。其次,这些材料通过设计特定的结合位点来提高检测系统的选择性,这些结合位点可以根据目标气体分子的化学性质(如大小、形状和官能团)选择性地识别目标气体分子。气体选择性捕获材料可以作为多孔材料存在,如沸石、金属有机框架(mof)和多孔聚合物,或者作为表面功能化的金属纳米颗粒。例如,Qiao及其同事(Qiao et al. 2018)展示了一个基于mof的VOC气体检测SERS平台(图6c-i)。为了提高气体生物标志物对肺癌早期检测的吸附,将ZIF-8层应用于金超颗粒(GSP)的自组装上,以降低气体生物标志物的流速,并减少GSP表面周围电磁场的衰减(图6c-ii)。气体醛是肺癌的指示器,通过ZIF-8通道被引导到sers活性GSPs底物上。然后通过希夫碱与预接枝到金GSPs上的4-氨基噻吩反应捕获气态醛,从而产生10 ppb的检测限。结合机器学习算法,该平台可以区分肺癌和健康肺呼吸(图6c-iii, iv, v),可作为早期肺癌的体外诊断工具。
电nic VOC气体检测
The technique of detecting VOCs using electrical signal output has gained significant interest due to the lack of necessity for light sources and detectors. Representative methods include acoustic wave devices (AWDs) based on the piezoelectric effect (Chen et al. 2018; Dou et al. 2018; Zhang et al. 2018), semiconductor metal oxide (Lin et al. 2019), and two-dimensional materials (Sun et al. 2018). The AWD typically consists of a piezoelectric substrate and a sensing film that is coated on the surface of the substrate (McGinn et al. 2020). When an electrical signal is applied to the piezoelectric substrate, it generates an acoustic wave that propagates through the substrate and the sensing film. The sensing film is designed to selectively interact with specific gas molecules, causing a mass-loading effect that alters the resonant frequency of the device. As VOCs interact with the sensing film, they are adsorbed onto the surface, causing a change in the mass of the film, and altering the resonant frequency of the device, referred as to the gravimetric sensing mechanism. This change in frequency is detected and measured by the device, providing information about the presence and concentration of the VOCs. For instance, Lu et al. (Lu et al. 2015) conducted a study where they developed four film bulk acoustic resonators (FBARs) with an ultrahigh operating frequency of 4.4 GHz to detect VOC gases (Fig. 7a-i, ii, iii). Each resonator was coated with a different supramolecular monolayer as the sensing film, namely p-tert-butyl calixarene (Calixarene), 2, 3, 7, 8,12, 13, 17, 18-octaethyl-21H, 23H-porphine (Porphyrin), β-cyclodextrin (β-CD), and cucurbituril (CB). The supramolecular monolayer coatings facilitated fast and reversible detection of VOCs by allowing the monitoring of the gas-phase “host-guest” interaction with the high-frequency FBAR sensor vibrating at 4.4 GHz (Fig. 7a-iv, v). This study highlights the potential of supramolecular coatings to enhance the performance of sensors for gas detection applications. Notably, gas selective adsorption films play a crucial role in gas sensors, offering several primary functions and benefits (McGinn et al. 2020). First and foremost, these films are designed to enhance selectivity. Through tailoring their composition, gas selective adsorption films exhibit a strong affinity for the specific gas species of interest, ensuring that only the desired gas molecules are adsorbed. This selectivity enhancement enables the sensor to accurately detect and quantify the target gas. Furthermore, gas-selective adsorption films contribute to sensitivity improvement. By preferentially adsorbing the target gas molecules onto their surface, these films amplify the sensor's sensitivity, allowing for the detection of even trace amounts of the gas. Additionally, these films aid in mitigating interference caused by other gases present in the surrounding environment. They are engineered to minimize or suppress the adsorption of interfering gases, thereby reducing their impact on the sensor's accuracy and specificity. Finally, gas selective adsorption films are characterized by their stability and repeatability in gas adsorption. Their engineered composition ensures long-term stability and reversibility, enabling consistent and reliable performance of the gas sensor over-time. Semiconducting metal oxides (SMOs) are widely used for VOC detection due to their high sensitivity and low cost (Steinhauer 2021). The basic mechanism of SMO sensors for VOC detection involves the change in the electrical conductivity of the sensor material in the presence of target VOC molecules. The sensor material is typically a metal oxide, such as tin dioxide (SnO2) (Fazio et al. 2021), tungsten oxide (WO3) (Modak et al. 2023), or zinc oxide (ZnO) (Pargoletti and Cappelletti 2020), that is highly sensitive to changes in the ambient environment (Ou et al. 2022; Pargoletti and Cappelletti 2020). When the sensor material is exposed to VOCs, the molecules are adsorbed onto the surface of the metal oxide, leading to a change in the electrical conductivity of the sensor material. This change in conductivity is due to the interaction between the adsorbed molecules and the free electrons in the metal oxide lattice. The presence of VOCs increases the number of free electrons, which in turn increases the conductivity of the sensor material. The change in conductivity can be measured by applying a small voltage across the sensor material and measuring the resulting current. The magnitude of the current is proportional to the concentration of the target VOC in the ambient environment. By monitoring the change in conductivity over time, the sensor can detect the presence of VOCs and provide information on their concentration. For instance, Li et al. (Li et al. 2017) prepared SnO2 microspheres for formaldehyde gas sensing by a simple hydrothermal method (Fig. 7b-i, ii). Upon exposure to the testing gas atmosphere, the sensor surface absorbed oxygen species which in turn captured free electrons from the sensing materials. This process resulted in the ionization of SnO2 microspheres to adsorbed oxygen ions at grain boundaries. The results show that the sensor has a response value of 38.3 to 100 ppm formaldehyde at an operating temperature of 200 °C, and the detection limit reaches 1 ppm (Fig. 7b-iii).
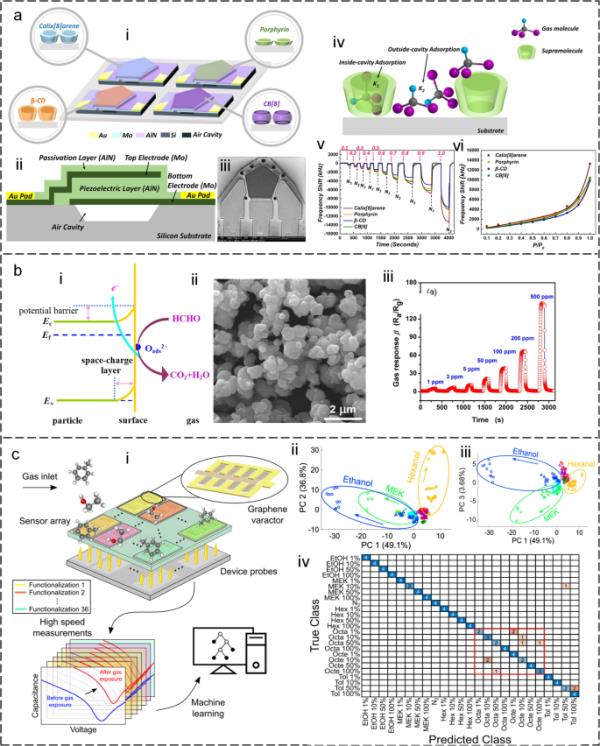
挥发性有机化合物气体检测的电方法学。使用基于重力机制的声学谐振器进行VOC气体检测(Lu et al. 2015)。i:四层超分子单层功能化的FBAR传感器阵列示意图。ii:器件部分示意图。iii:设备的SEM图像。iv: VOCs吸附示意图。v:暴露在氯仿气体中的FBAR传感器的实时响应。vi:氯仿吸附等温线。b使用半导体金属氧化物检测VOC气体(Li etal . 2017)。i: HCHO检测传感器的反应机理。ii:合成SnO2微球的SEM图像。iii: SnO2微球气体传感器动态响应-恢复曲线。c用于VOC气体检测的机器学习石墨烯电子鼻(Capman et al. 2022)。i:基于ml的传感器系统原理图。ii: PCA评分图,显示测量响应在主成分1和主成分2上的投影。iii:混淆矩阵
为了能够精确测量多种气体,各种气感膜和人工智能算法辅助的阵列设计的组合显示出巨大的潜力(Barucha et al. 2022;Yang et al. 2018)。Capman等人(Capman et al. 2022)展示了使用基于石墨烯的可变电容器阵列选择性和快速检测多种挥发性有机化合物(图7c)。石墨烯与不同化学受体的功能化使得包含108个传感器和36个化学受体的交叉选择性阵列得以发展。从108个传感器采集的多路复用数据在数十秒内完成,从而可以快速测量voc。尽管与快速测量相关的信号幅度降低,但该方法在检测五种被测分析物(乙醇、己醛、甲基乙基酮、甲苯和辛烷)时显示出98%的显着准确性。添加1-辛烯,一种结构与辛烷高度相似的分析物,导致准确度略微降低到89%。这些发现表明,基于石墨烯的变容二极管阵列具有选择性和快速检测不同浓度的多种挥发性有机化合物的潜力。
此外,光学和电学VOC检测方法各有优势。挥发性有机化合物气体检测的光学方法具有高灵敏度、优异的选择性和快速的响应时间(Khan et al. 2020)。它们能够检测十亿分之一(ppb)的低气体浓度,使它们适合需要高灵敏度的应用。使用特定波长的光可以从干扰气体中区分目标气体,从而提高选择性。光学方法还提供实时或近实时监控功能,响应时间通常在秒或毫秒量级。然而,它们可能容易受到环境因素的干扰,并且由于专门的光学元件,它们可能更昂贵。另一方面,电方法在百万分之一(ppm)范围内表现出良好的灵敏度,并为传感器设计提供了灵活性(McGinn et al. 2020)。它们可以集成到紧凑的便携式设备中,允许个人监控或手持应用。虽然与光学方法相比,电方法的灵敏度可能略低,但它们可以通过使用传感器阵列和模式识别技术来提高选择性。电方法通常具有更快的响应时间,并且对环境干扰更有弹性。然而,它们可能需要定期校准或更换传感材料,并且它们的选择性可能对单个传感器有限。最终,选择光学方法还是电气方法取决于具体的应用要求、目标气体特性和成本考虑。
人工智能增强VOC平台
人工智能算法对VOC气体检测越来越重要,因为它们对VOC传感器有好处(Haripriya et al. 2023;Lekha和Suchetha 2021;Lotsch et al. 2019;Mahmood et al. 2023;Thrift等人,2019;Zhou et al. 2021;周海,等。2023a)。首先,机器学习算法的使用促进了挥发性有机化合物传感器的自动化设计,从而消除了费力而耗时的设计过程。这在SEIRA天线的设计中得到了体现,该天线涉及分析被分析物分子的红外光谱,并随后选择合适的天线结构以匹配分子振动频率。设计过程涉及关键和重复的优化过程,包括结构形状的选择,天线尺寸的调整,以及纳米制造限制的考虑。人工智能辅助设计系统有效地处理这些任务,从而产生更有效和高效的设计结果。例如,Li及其同事(Li, D. et al. 2021a, 2021b)在2021年使用基于遗传算法(GA)的AI方法开发了一种用于COVID-19检测的敏感SEIRA底物(图8a-i)。目前可用的新冠肺炎诊断方法,如RT-PCR、血清学测试或胸部计算机断层扫描,都有其局限性,例如灵敏度低且程序耗时。发展等离子体方法进行即时诊断是非常可取的。基于ga的人工智能方法采用从红外光谱中提取分子复介电常数作为分子振动行为建模的第一步。随后,该遗传算法从多设计参数问题中快速识别出灵敏度高、等离子体共振和分子振动零失谐、增强系数高的最优解(图8a-ii)。此外,SEIRA方法可以通过比较病毒峰值的强度和频率来区分COVID-19突变,这对传统诊断方法提出了重大挑战。
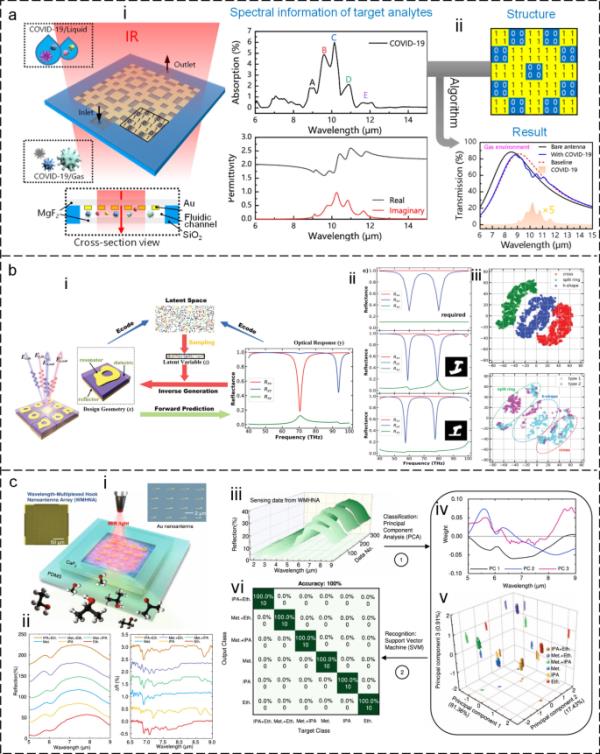
人工智能增强的传感器设计和VOC检测。基于机器学习的传感器正向设计(Li, D. et al. 2021b)。i:传感器3D视图。ii:设计过程。b使用半监督深度学习算法的传感器逆设计(Ma et al. 2019)。i:逆设计原理图。ii:期望光谱(上图),反设计结果(下图)。插图是通过算法实现的设计模式。iii:潜在空间的可视化。c机器学习支持VOC检测(Ren et al. 2022)。i: VOC传感器示意图。ii:分析物的实测光谱显示出光谱重叠,用经典的数据处理方法很难区分清楚。iii:实测的原始光谱数据。iv:采用PCA对数据进行预处理。v:各谱在三维空间中得分的权重。vi:分析物分类结果的混淆图
除了上述的正向设计之外,AI算法还可以用于反向设计,通过使用标记和未标记的数据来减少训练数据量(Liu et al. 2018)。Ma等人(Ma et al. 2019)提出了一种独特的反设计网络,该网络利用预定义的基于分布的潜在变量对输入几何形状的结构设计和光学响应进行编码(图8b-i)。可以对潜在变量进行随机采样和解码,以重建原始结构几何形状,从而实现逆设计。从反设计参数(图8b-ii中、下窗格)得到的模拟光谱与所需光谱(上窗格)非常吻合。采样过程对相同的目标光谱产生不同的输出,从而产生反向设计的多个候选。此外,所提出的模型可以通过对标记和未标记数据进行编解码训练迭代来学习区分各种形状(图8b-iii)。
人工智能算法可以以快速、直接和自动化的方式促进VOC传感器对数据的分析和处理(John-Herpin et al. 2021;Kuhner et al. 2019)。通过降维,缓解了海量光谱数据带来的压力。在实时监测应用中,输出数据由三维信息组成,包括光谱强度、波长和时间。如果目标是多个分析对象,则信息变成四维的,其中包括类别信息。这导致了大量的光谱数据,光学方法难以准确、快速地分析和处理。在其他ML算法中,PCR可以在保留特征的同时降低信息的维数。这导致了数据量的减少,数据处理的简化,以及测试结果的快速生成。随着传感器技术的进步和气体数量的不断增加,可以预见,数据量将不可避免地增加。因此,使用ML算法对光谱数据进行降维是对VOC传感器的宝贵帮助。Ren et al. (Ren et al. 2022)设计了一种利用波长复用技术对指纹区多个吸收峰进行连续宽带检测的钩形纳米天线阵列(图8c-i)。具有相似官能团的不同分析物的SEIRA光谱往往在许多区域重叠,导致难以在与窄带SEIRA底物的混合物中区分它们(图8c-ii)。然而,通过PCA和SVM算法的结合,作者对甲醇、乙醇和异丙醇的识别准确率达到了100%,如图8c-iii-vi所示。采用适当的预处理技术将原始传感器数据转换为更适合学习算法的格式和信息(Guo, K. et al. 2021a)。传感器数据的预处理包括几个关键步骤。首先,执行数据清洗以解决传感器读数中的缺失数据、异常值和噪声。缺失的数据可以通过一些技术来处理,比如均值输入、插值或专门为处理缺失数据而设计的机器学习算法。其次,数据归一化或缩放技术,如最小-最大缩放或z分数归一化,用于解决传感器数据中观察到的尺度和范围的变化,因为这些会影响机器学习模型的性能。通过将所有的特征放在一个相似的尺度上,这些技术可以确保没有单一的特征主导学习过程。此外,特征选择或提取方法用于从传感器数据中存在的潜在大量特征中识别最相关的特征。相关分析、互信息或特征重要性度量等技术通常用于此目的。最后,将预处理后的传感器数据分为训练集、验证集和测试集。训练集用于训练机器学习模型,验证集辅助调优超参数,测试集用于评估训练模型的最终性能。总的来说,人工智能技术的进步为通过快速传感器设计和自动化数据处理来增强VOC传感器提供了广阔的潜力,从而使它们能够有效地应对未来的挑战。此外,物理知识可以提高算法的性能,降低优化难度。例如,Khatib等人证明,将基础物理知识作为输入,并在训练过程中对这些量进行预训练,有可能提高网络性能,并减轻与优化相关的挑战(Khatib等人,2022)。该模型能够准确预测感兴趣的光谱,并与目标光谱一致,这证明了深度神经网络在优化VOC气体传感器设计方面的有效性。此外,训练后交叉验证集计算的均方误差作为评估模型预测精度的有价值指标。
人机接口
传感器技术的快速发展已经成为工业4.0背后的推动力(Wang, T. et .2018c;Zhou et al. 2015;Zhu et al. 2019)。能够检测物理刺激或化学变化并作出反应的传感器使各种系统能够实时收集和处理数据,如用于视觉感应的摄像头和用于语音识别的麦克风。基于mems的传感器,如加速度计、陀螺仪、压力传感器、触觉传感器和生物传感器,由于其众多优点,包括小尺寸、低功耗、低成本、高可靠性和鲁棒性,在许多应用中,特别是在可穿戴电子产品中,已经被广泛使用(Erdil et al. 2022;Liu et al. 2013;Manvi and Mruthyunjaya Swamy 2022;Pitchappa et al. 2015;Yazici et al. 2020)。人工智能数据分析与可穿戴传感器的集成可以捕获关键信息,如肌肉变形、关节弯曲、温度变化和心跳频率。这些数据对于包括医疗保健、环境监测、人机交互(HMI)和智能城市在内的广泛应用都是非常宝贵的。通过利用先进的传感器技术和人工智能数据分析,可穿戴设备可以提供实时洞察,促进更明智的决策并提高各种应用程序的效率(Han等人,2018;刘辉等,2020b;Wang, Y.等,2021)。
触觉传感器
接下来的例子旨在强调结合触觉传感器的重要性。如图9a (Sundaram et al. 2019)所示,Sundaram等人提出了一种价格合理且可扩展的触觉手套(STAG),能够进行物体识别、重量估计和手部姿势识别。STAG包括一个带有584个压阻传感器的传感套,一个针织手套,以及利用ResNet-18架构训练模型并最终识别26个不同物体的读出电子设备。这些方法表明,由于柔性电子元件的进步和DL技术的支持,可以在更深刻的层面上获得大量信息,从而促进下一代可穿戴电子产品和系统的未来设计和开发。
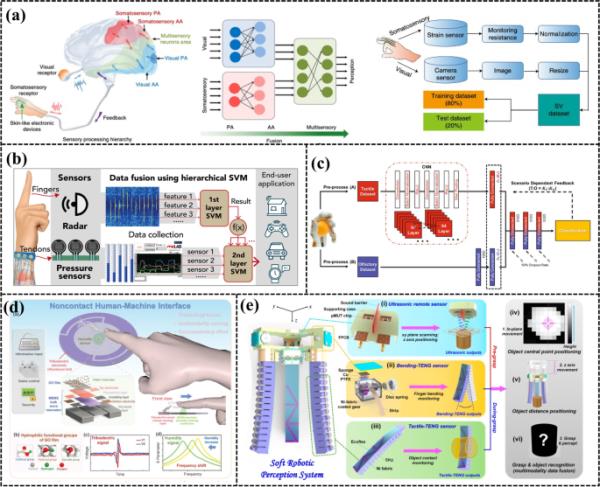
先进的人工智能增强可穿戴手套传感器。a可伸缩触觉手套(STAG)由带有584个压阻传感器的传感套组成(Sundaram et al. 2019)。b一种柔性的四重触觉传感器,用于机器人手部感知抓取的物体(Li et al, 2020)。c一种基于独特纱线结构的TENG应变传感器,用于智能手套应用(Zhou, Z. et al. 2020b)。d结合超疏水摩擦电纺织品传感器的低成本、自供电、直观的手套式人机界面(Wen, F. et . 2020a, 2020b, 2020c)。e基于TENG手套的手语识别与交流系统(Wen, F. et al. 2021)
如图9b所示,Li等人开发了一种柔性的四层触觉传感器,使机器人手能够感知不同材料和形状的抓取物体,并进一步采用具有三层隐藏层的多层感知器(MLP)来实现自动废物分类。触觉传感器的设计包括两个传感层,每层都有两个传感元件,包裹着一个多孔的银纳米粒子注入的聚二甲基硅氧烷(PDMS)。顶部和底部热膜分别响应接触物体的导热系数和施加的压力,受不同材料的导热系数变化和多孔物质变形引起的导热系数变化的影响。冷膜作为局部温度传感器,识别物体和环境温度。触觉传感器可以同时检测多个刺激,交叉耦合误差可以忽略不计,提供与物体相关的更有洞察力的特征,提高机器学习过程中的识别精度。因此,它证明了其在大幅减轻个人对智能家居环境保护和可持续发展的负担方面的潜力。
增高HMIs
与传统和流行的电阻式和电容式传感器相比,压电传感器和摩擦电传感器可以在机械变形时产生自产电压,无需外部电源。Zhou等人提出了一种基于独特纱线结构的TENG应变传感器,如图9c所示(Zhou, Z. et al. 2020b)。传感器单元的核心包括一根导电纱,绕着一根橡胶超细纤维,所有这些都被封装在PDMS套筒内。不同程度的变形导致PDMS套筒和卷曲导电纱之间的接触面发生稳定和持续的变化,使传感器在宽应变范围内(20-90%)具有显著的线性和灵敏度。一旦集成了无线印刷电路板(PCB)进行信号采集、处理和传输,就可以使用多类支持向量机算法开发可穿戴的符号-语音转换系统。系统总体精度保持在98.63%以上,响应时间短(小于1秒)。这显示了一种经济的方法,可以使使用手语的个体和不使用手语的个体之间进行交流,并且还突出了基于teng的HMI在医疗保健环境中的潜在应用。
此外,将超疏水摩擦电纺织品传感器与ML结合,开发了一种低成本、自供电、直观的基于手套的人机界面,如图9d所示(Wen, F. et al. 2020a, 2020b, 2020c)。这种创新的设计允许在真实和虚拟空间中进行复杂的手势识别和控制,同时最大限度地减少湿度和汗水对性能的负面影响。碳纳米管/热塑性弹性体(CNTs/TPE)涂层方法用于制造超疏水纺织品,从而提高能量收集和人体运动感应能力。与原始纺织品相比,这种纺织品从高湿度环境中恢复的时间更快,摩擦电性能提高了三倍,并且具有更好的生物力学能量清除能力。基于手套的人机界面,通过机器学习增强,显示出96.7%的高识别准确率,优于非超疏水系统(92.1%)。即使在运动一小时后,它也能保持80%的电压输出。开发的手套界面已成功应用于各种虚拟现实/增强现实(VR/AR)控制,包括射击游戏,棒球投球和插花。
此外,基于手套的手势识别系统在帮助语言和听力受损者方面具有巨大的潜力,特别是在手语识别方面。人工智能手套系统可以实时有效地识别和翻译各种手语手势,为语言和听力障碍人士提供无缝沟通。此外,这些先进的系统可以通过在不同和广泛的数据集上进行训练来进一步完善,提高其准确性和识别能力,以便在各种应用中识别复杂手势的通用平台。因此,如图9e所示,Wen等人展示了一种基于智能手套传感器的手语识别和交流系统(Wen, F. et al. 2021)。深度学习算法首先对词成分进行识别,然后对原句子进行重构,准确率分别达到82.81%和85.58%。此外,分割方法为识别新的或以前未见过的句子开辟了新的途径。具体来说,已识别的单词单位可以重新组织成不同的顺序来构建新的句子。同时,深度学习模型识别新句子中的所有基本单词元素,并建议适当的翻译。通过这种方式,可以识别未包含在训练数据集中的句子。最后,句子识别结果在虚拟空间中可视化,手语使用者可以使用他们熟悉的语言进行交流,而非手语使用者可以通过他们控制的VR界面直接输入。这一在识别现有和新句子方面的突破提高了手语识别系统的实用性,标志着向最大限度地减少手语使用者和非手语使用者之间的交流障碍迈出了重要的一步。
人工智能增强的多模传感器
多模态提供了许多好处,包括提高准确性、冗余性、补充信息、适应性、鲁棒性、增强的功能和可扩展性(Sun et al. 2021;Shih et al., 2020)。这些优势使智能传感器系统成为机器人、环境监测、医疗保健和安全等各个领域的重要组成部分,在这些领域,可靠和全面的信息对于有效的决策和性能至关重要,使智能家居能够做出明智的决策和定制化的行动。如图10a所示(Wang, M. et al. 2020a, 2020b, 2020c),设计了一种生物启发的数据融合架构,将视觉数据与来自类皮肤可拉伸应变传感器的体感数据相结合,进行人体手势识别。应变传感器由单壁碳纳米管制成,学习架构利用CNN进行视觉处理,然后利用稀疏神经网络进行特征级传感器数据融合和识别。这种数据融合方法实现了100%的恒星识别精度,同时在图像传感器的非理想条件下(如噪声、曝光不足或过度曝光)保持这种精度。以机器人手势导航为例,说明了该数据融合方法的稳定性,光照条件下的误差范围为1.7%,黑暗条件下的误差范围为3.3%。

多模态传感器和基于ml的数据融合。a Bioinspired数据融合架构,通过整合视觉数据和来自皮肤可拉伸应变传感器的体感数据(Wang, M. et al. 2020a, 2020b, 2020c)。b雷达和压力传感器的HSVM算法(Liang et al. 2019)。c一种受鼹鼠启发的嗅触觉相关机器学习架构(Liu, M. et al. 2022c)。d结合MEMS湿度传感器和摩擦电传感器的多模态非接触式人机界面(Le et al. 2022)。e集成了超声波传感器和柔性摩擦电传感器的软机器人感知系统(Shi et al. 2023)
此外,图10b中提出了一种使用分层支持向量机(HSVM)算法的多传感器数据融合新方法(Liang et al. 2019)。它采用了一种创新的学习系统,融合了雷达技术来跟踪手和手指的运动,以及一组多功能的压力传感器,确定手腕周围的压力分布。为了有效地合并不同的数据类型,我们设计了HSVM框架。它考虑了各种因素,包括采样率,数据架构,以及来自压力传感器和雷达的复杂手势数据。通过分析从15个参与者收集的数据集,可以观察到,独立雷达技术的平均分类准确率为76.7%,而单独使用压力传感器的准确率为69.0%。然而,当实现HSVM算法时,我们注意到一个显著的改进,因为它结合了压力传感器和雷达的输出,将分类准确率提高到值得称赞的92.5%。
此外,提出了一种仿生嗅觉触觉(BOT)相关的机器学习架构,通过处理多模态数据和(图10c)来实现目标识别(Liu, M. et al. 2022a)。与BOT相关联的设计结构是CNN、MLP和决策神经网络的组合。该结构中CNN的任务是生成与压力数据对应的512维特征向量。相反,多层神经网络旨在创建与嗅觉数据一致的100维特征向量。决策神经网络将这两个特征向量合并为一个612维特征向量,并进行关联学习,实现高精度的目标识别。这一过程证实了合并来自各种传感器类型和机器学习算法的多模态数据可以导致高精度,宽容的学习系统的发展的断言。这种系统非常适合于复杂环境中涉及高精度目标识别和决策的任务。图10d显示了一个极简、低功耗、多模态的非接触式人机界面,它结合了一个MEMS湿度传感器和一个摩擦电传感器(Le et al. 2022)。当前的非接触式人机界面面临着诸多挑战,包括过度的功耗、复杂的信号处理电路以及缺乏对多维交互的支持。然而,这种新的人机界面通过融合来自两个传感器的互补信息来克服这些问题。该MEMS湿度传感器采用氮化铝(AlN)体波谐振器和氧化石墨烯(GO)薄膜,体积极小,具有高信号强度和低信号噪声水平,可以在手指靠近时与手指进行持续稳定的交互。这种摩擦电传感器由两个环形铝电极组成,可以快速识别手指在多个方向的运动。通过结合这些传感器,提议的界面可以用作VR的游戏控制界面和高安全性3D密码的密码输入界面,显示出其在即将到来的虚拟世界中无数应用的潜力。湿度传感器具有高灵敏度,低信号噪声,卓越的重复性,快速响应和恢复速度,而摩擦电传感器提供补充跟踪多向和动态手指运动。未来的应用可能渗透到虚拟世界的可穿戴领域,采用柔性或纺织基板作为基础平台。
此外,施。Shi et al. 2023开发了一种软机器人感知系统,该系统集成了超声波传感器和柔性摩擦电传感器,可实现远程目标定位和多模态认知(图10e)。该系统解决了依赖相机或光学传感器的传统制导系统的局限性,包括对不同环境适应性差、数据复杂性增加和成本效率低下等挑战。利用反射超声,超声波传感器识别物体的形状和距离,从而使机器人机械手能够定位自己适合物体捕获。随着抓取阶段的展开,超声波和摩擦电传感器的组合收集各种感官数据,如物体的上轮廓、尺寸、形状、刚度和材料构成。这些数据随后通过深度学习进行合并和分析,从而大大提高了物体识别的准确性(高达100%)。所提出的感知系统为软机器人中定位能力与多模态认知智能的融合提供了一种简单、经济、高效的策略。它显著拓宽了当前软机器人系统在工业、商业和消费者应用中的功能和适应性,展示了在物联网和人工智能时代自动分拣、无人商店和医疗保健援助方面的巨大潜力。
人工智能增强的自我可持续系统
除了手套传感器,脚上的传感器还可以为医疗保健和个人识别应用提供有价值的信息。基于teng的步行设备可以结合能量收集和步态分析的功能来创建一个自供电系统(Aqueveque et al. 2020;Han et al. 2019)。虽然鞋垫通常用于能量收集和步态传感,但袜子可能提供更舒适、更灵活的选择,特别是在不穿鞋的室内场景。如图11a所示,Zhang等人开发了基于TENG的智能袜子,其设计不仅可以捕获和重新利用低频身体运动产生的浪费能量,还可以无线传输感官数据(Zhang, Z. et al. 2020)。此外,这些可穿戴传感器可以收集并提供有关佩戴者身份、健康状况和活动水平的重要信息。在动态步态周期中收集的原始数据直接输入1D CNN模型进行训练,不需要复杂的预处理步骤。这款智能袜子配备了多像素传感器阵列,能够从足部运动中积累大量信息,从而实现复杂的步态分析,并有可能在更广泛的用户群体中提高准确性。在识别13种单独的步态模式时,准确率达到了93.54%。通过采用深度学习分析,智能袜子有可能在智能建筑中营造更安全、更智能的环境,从而消除对摄像头和麦克风的需求。
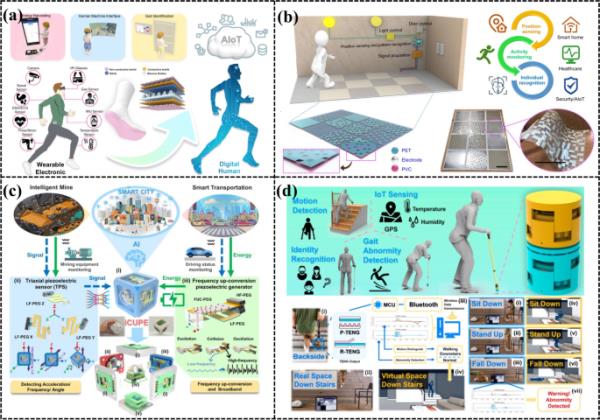
人工智能增强的物联网(AIoT)应用自我可持续系统。a具有能量收集和步态传感功能的低成本摩擦电袜(Zhang, Z. et al., 2020b)。b具有深度学习功能的智能垫,具有位置/活动感知和个体识别功能(Shi, Q. et al. 2020b)。c用于智能采矿、工厂自动化、交通和智能城市应用的自供电压电AIoT节点(Huang et al. 2023)。d一种用于老年人护理的多功能手杖(Guo, X. et al. 2021b)
除了使用智能袜子进行步态分析之外,另一种常见的技术包括使用基于地垫的传感器。Shi等人提出了一种支持深度学习的智能垫(DLES-mat)阵列,能够进行位置/活动感知和个体识别,如图11b所示(Shi, Q. et al. 2020b)。由于每个人走路的步态模式都是独一无二的,当一个人在摩擦电DLES-mat阵列上行走时,就会产生独特的输出电压模式。当一个人穿过DLES-mat阵列时,来自人体步骤的周期性接触分离运动在两个传感电极上产生摩擦电输出信号。基于cnn的深度学习模型获得了较高的识别性能,准确率达到96.0%。训练后的模型在基于相似步态模式的身份识别的实时控制方面具有重要的潜力。DLES-mat被描绘成一个复制真实走廊的虚拟走廊环境中的数字孪生系统,反映了用户的实时状态。这包括通过峰值检测的位置感知和通过深度学习预测的个人识别。与经常引起隐私问题的基于摄像头的监控系统相比,这种智能地板监控系统在虚拟环境中采用个人的数字孪生,仅显示位置信息和可识别的身份,这对自动化、医疗保健和安全应用至关重要。
此外,Huang等人设计了一个自供电的压电AIoT节点,命名为iCUPE(图11c) (Huang et al. 2023)。iCUPE围绕三维(3D)六面体模块化结构建造,体现了具有AIoT功能的自我可持续系统。它包含六个可互换的模块,每个模块都有独特的功能,并战略性地定位在它的六个面。这些模块包括温度和湿度传感模块、蓝牙通信模块、数据处理中心单元和变频压电发生器(FUC-PEG)模块。FUC-PEG模块的作用是通过将低频压电发生器(LF-PEG)与厚膜高频压电发生器(HF-PEG)结合起来,拓宽iCUPE的频率带宽。该模块将低频输入转换为高频自振荡,从而在低频条件下产生48 V的开路电压。值得注意的是,iCUPE无需外部电源,就能捕获环境中的振动信号,从而产生频率和加速度等初步数据点。一种结合机器学习的自供电三轴压电传感器(TPS)利用低频压电发生器(lf- peg)将三个正交的压电传感单元集成在一起。这种集成实现了高精度,多功能振动识别,加速度分辨率为0.01g,频率分辨率为0.01 Hz,倾斜角分辨率为2°。因此,TPS可以达到很高的识别准确率,范围在98%到100%之间。
为了满足全球老年人口和行动障碍人群的需求——这一人口数量已经超过10亿,并且还在不断增加——我们提出了一种多功能手杖,如图11d所示(Guo, X. et al. 2021b)。这种创新的手杖由两个主要功能单元组成:杂交单元和旋转单元。该混合模块包括顶部按压TENG (P-TENG)、中间位置肌电图和底部旋转TENG (R-TENG),可跟踪压力动态。P-TENG由铝、腈和Ecoflex分层而成,可根据施加的压力产生可变电压。它的底部铝层分为五个电极,记录了手杖与地面从接触到释放的整个互动过程。通过1D-CNN深度学习结构分析P-TENG输出,操纵杆识别五种不同的动作(上升、坐下、行走、上升和下楼梯),评估三种不同的状态,并识别十个不同的用户。另一方面,R-TENG通过监测输出信号来标记不寻常的步态模式,比如摔倒。一个人工智能驱动的虚拟环境,旨在模仿现实世界的场景,准确地代表了用户的实时运动。P-TENG和R-TENG的输出信号由单片机模块采集,无线发送到计算机进行解读。深度学习模型捕捉用户在家中的实时运动状态,并将其映射到虚拟环境中。如果发生坠落,异常立即被检测到,允许快速呼叫帮助。与传统的室内健康监控系统不同,这款手杖通过只关注用户的运动状态作为健康指标来优先考虑隐私。它的设计捕捉了那些行动不便的人的超低频率运动,将低频线性运动转化为高速旋转。收集的机械能为具有GPS跟踪和环境温湿度传感功能的自我维持物联网系统提供动力,确保全面的用户监控。这种AIoT的创新集成使手杖成为移动和健康监测的有效工具。
下载原文档:https://link.springer.com/content/pdf/10.1186/s42234-023-00118-1.pdf

