摘要
为在碱性直接甲醇燃料电池中寻找合适的电催化剂,人们正在进行重要的研究。尽管取得了巨大的进步,但生产具有高活性和高稳定性的非铂催化剂仍然很困难。本文采用共溅射沉积方法,利用不同的沉积时间(200,400,600和800)秒,在氟掺杂氧化锡(FTO)上沉积了掺银NiO薄膜。随着沉积时间从200、400、600到800)秒的增加,沉积膜的厚度从17、35、70和100 nm不等。NiO-Ag-800的带隙最小,为3.36 eV,而NiO-Ag-200的带隙最大,为3.81 eV。所制备的薄膜被用作甲醇氧化的电催化剂。它的物理性质有利于吸附反应,使电解质更容易渗透,并有助于快速反应动力学。此外,由于Ag-NiO沉积在FTO衬底上,具有出色的附着力和良好的电接触,因此可以利用;不添加任何粘合剂或导电剂。该薄膜显示出甲醇氧化电位降低,电流密度高,长期稳定性好。薄膜的厚度证明了它在电活动中起作用。薄膜的效率随厚度的增加而增加,其中Ag - nio -800记录的最低起始电位为0.37 V vs Ag/AgCl。
1 介绍
由于技术使用的巨大发展,这取决于电力,化石燃料被高度消耗来发电;此外,它还会对环境产生负面影响[1,2]。因此,研究人员致力于开发清洁、可再生、有效、环境可接受的替代能源来满足不断扩大的能源需求[3]。其中,以甲醇为燃料的直接甲醇燃料电池(direct methanol fuel cells, DMFC)因其成本低、环保、易操作等优点,已成为一种可替代的发电方法[4]。然而,dmfc存在甲醇交叉困难、耐久性降低、稳定性差、热和水控制困难以及生产成本高等问题,因此不希望商业化[5]。许多研究人员已经用各种尖端方法解决了甲醇氧化燃料电池运行的困难[6,7,8,9]。在酸性和碱性介质中开发低成本、高性能的氧还原反应(ORR)非贵重电催化剂的试验较多,这是清洁能源发电的迫切需要[10,11,12,13,14]。
电催化剂的选择对甲醇燃料电池的性能有显著影响[15]。虽然铂和贵金属基电催化剂在燃料电池应用中得到了广泛的应用[16],但它们是造成成本高和一氧化碳中毒的主要原因。因此,研究人员转向基于非贵金属过渡金属氧化物的电催化剂,展示了提高电催化活性的有效策略,提供了有希望的替代催化剂[17]。其中,NiOx[18]、CoOx[19]、CuOx[19]、CrOx[20]、MnOx[21]和FeOx[22]催化剂表现出增强的反应动力学和优异的抗中毒潜力。由于镍(Ni)是一种经济、丰富的非贵金属,镍基催化剂已广泛应用于许多传统工业催化过程中,包括甲烷重整[23]、加氢反应[24]、加氢裂化反应[24]和氧化反应[25]。此外,在催化过程中,Ni表面发生氧化还原反应,产生Ni (OH)2和NiOOH,这被认为是甲醇分子在碱性电解质中的活性反应位点[26]。
催化剂的形态和晶体结构对其催化活性有显著影响[2]。纳米技术已经被证明在开发更高效的催化剂方面是有用的[1]。镍基材料的不同纳米结构的合成技术多种多样,包括原子层沉积[27]、溶胶-凝胶化学沉积[28]、喷雾热解[29]、水热法[30]等。尽管有了相当大的改进,但大多数制造过程必须简化以用于工业用途,或者需要使用损害催化剂性能的化学品[31]。此外,许多镍基催化剂由于相变、结构解体以及催化剂与导电衬底之间的粘附性差,导致长期耐久性差,导致材料损失[32]。由于氧化镍极易溶于大多数典型的碱性电解质,因此对材料的结构和形态保持足够的控制是一项挑战[33]。
掺杂可以进一步提高电化学活性,因为它会影响电子结构,这是提高电催化活性的关键因素。此外,添加杂质可以在接收材料内部产生可电离的原子[34,35]。许多元素都能影响电催化活性,但所选择的每一种元素都是用来达到特定的目的。因此,Ag在碱性环境中建立长期稳定性的能力已在多项研究中得到证实[36,37,38,39,40]。
本文通过共溅射沉积方法在FTO衬底上沉积了掺杂ag的NiO薄膜,并将其作为甲醇电氧化的电催化剂。据我们所知,使用这种材料的薄膜结构作为甲醇氧化的电催化剂的工作还没有报道。制备的掺银NiO膜具有表面粗糙、厚度合适的特点,延长了沉积时间,有利于电解液的吸附,使离子扩散更大,提供了不同的活性位点。由于掺银NiO薄膜生长在像FTO一样具有很强附着力的衬底上,所以掺银NiO可以直接用作甲醇氧化的电催化剂,而不需要添加任何导电剂或粘合剂。
2 材料与方法
2.1 样品制备
共溅射沉积法是调节和监测载体薄膜中掺杂原子数量的重要方法之一。我们使用DC/RF溅射设备(Syskey Technologies, Taiwan),通过不同的沉积时间从200、400、600到800 s,在玻璃载玻片和氟掺杂氧化锡(FTO)上沉积了3.53%的ag掺杂NiO薄膜,厚度分别为17、35、70和100 nm。在沉积前,用丙酮和乙醇清洗玻片和FTO,然后用氮气干燥。在样品制备过程中,Ni靶材的直流功率保持在200 W, Ag靶材的射频功率保持在20 W。其他沉积参数在沉积过程中保持恒定,如操作压力、衬底温度、衬底旋转、氧气流速和氩气流速分别为5 × 10−3 Torr、25℃、15 rpm、10 SCCM、20 SCCM。根据沉积时间的不同,将样品分别命名为NiO-Ag-200、NiO-Ag-400、NiO-Ag-600和NiO-Ag-800。
2.2 所制备薄膜的表征
利用40 kV/40 mA Cu-Kα辐射(0.154056 nm)下的x射线衍射(Shimadzu LabX-XRD-6000, Japan)测定薄膜的晶相。采用场发射扫描电子显微镜(FESEM, Zeiss sigma 500 VP,德国)检查形貌和结构。在FESEM上固定的能量色散x射线也被用来评估元素组成并绘制薄膜表面的成分图。用紫外可见分光光度计(Perkin Elmer Lambda 750;麻萨诸塞州,美国)。XPS记录了在K-ALPHA (Thermo Fisher Scientific, USA)上收集的制备薄膜的化学状态,其单色x射线Al K-ALPHA辐射为- 10至1350 eV,光斑尺寸为400 μm,压力为10 - 9 mbar,全谱通过能量为200 eV,窄谱通过能量为50 eV。
2.3 电化学测量
在室温条件下,通过三电极装置研究和评价了各制备薄膜在碱性溶液中对甲醇氧化的电催化活性。参考电极和对电极分别为Ag/AgCl和Pt丝,合成的薄膜作为工作电极。此外,电解质溶液中含有0.5 M KOH,使用了不同浓度的甲醇(0.5,1,2 M)。通过将估计的甲醇体积与KOH溶液相结合,评估了0.5 M KOH纯溶液和甲醇存在下的电催化活性。所有电化学实验均使用Autolab PGSTAT302N电位器(metrohomm)进行,扫描速率为5至100 mV s - 1的循环伏安法(CV)、0.6 V下1小时的计时电流法(CA)和0.6 V振幅为10 mHz的电化学阻抗谱法(EIS)。电流密度根据电极的几何表面积进行了标准化。
目录
摘要 1 介绍 2 材料与方法 3.结果与讨论 4 结论 数据可用性 参考文献 致谢 作者信息 道德声明 搜索 导航 #####3.结果与讨论
3.1 结构分析
用XRD对所制备薄膜的结晶度进行分析,结果如图1所示。ICDD卡[01-089-3080]与衍射峰相匹配,确定了三角结构氧化镍单相的空间基团R-3 m(166)。由于在氧化镍中添加的银量很少,所以没有形成与纯氧化镍(021)、(202)和(220)中发现的不同的峰。XRD分析结果表明,制备的NiO薄膜具有良好的结晶性和较高的纯度。
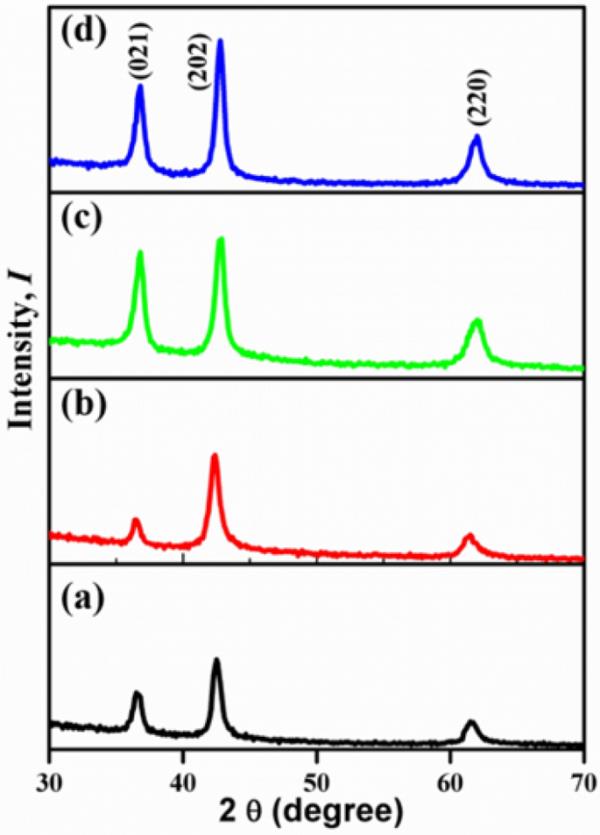
不同时间沉积NiO-Ag薄膜的x射线衍射
采用Debye Scherrer方程计算平均晶粒尺寸D。(第四十一条、第四十二条)。
(1)式中,D为晶体尺寸,λ为x射线所用波长,β为峰半峰全宽,θ为衍射角。同样,用式(2)和式(3)计算位错密度δ和晶格应变[35,43]。
(2) (3)表1给出了不同厚度薄膜的结构属性,包括平均晶粒尺寸、位错密度和晶格应变。结果表明,随着沉积时间的增加,薄膜的晶粒尺寸也有一定的变化,其中NiO-Ag 800的晶粒尺寸最大,为10.93 nm, NiO-Ag 200的晶粒尺寸为9.41 nm。由于在NiO - Ag薄膜中Ag的含量很低,所以三个衍射峰的位置非常接近文献中提出的纯NiO的位置[44]。沉积时间对所制备薄膜结晶度的影响不明显;这可能是由于所有样品的化学成分都是相同的,唯一的区别是厚度。然而,随着沉积时间的增加,制备膜的微观结构发生了明显的变化,在较厚的样品情况下,样品表面变得粗糙。此外,随着样品厚度的增加,出现了多孔结构构型,这有利于离子/电子的快速传递和对甲醇电氧化的电化学反应性增强。
3.2 x射线光电子能谱学
XPS光谱中核能级结合能的变化可以用来确定NiO-Ag的氧化态。图2a描绘了NiO-Ag-800复合薄膜的XPS测量光谱。c15、o15、Ag 33d /2和Ni 2p3/2谱线是光谱中的主要峰,其标准结合能分别为284.3、529.6、368.5和855.2 eV。NiO - ag -800样品在855.2 eV处有一个强峰,是NiO相的特征峰。Ni 2p3/2和2p1/2的核能级结合能分别为854.8和872.3 eV,如图2b所示。
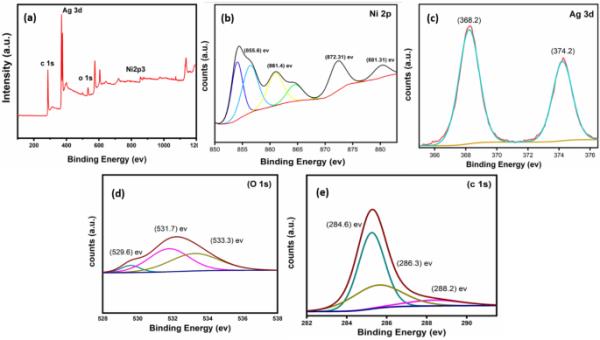
nio - ag800的XPS光谱,a测量光谱,b Ni 2p, c Ag 3d, d O 1s和ec 1s光谱
图2b将Ni 2p反褶积谱分别描绘为Ni+ 2 (NiO)和Ni+ 3 (Ni2O3)的双组分峰[45,46]。曲线显示了NiO (853.2 eV)和Ni2O3 (855.6 eV)这两种不同成分对氧化镍膜的反褶积作用。另外,在861.3 eV处有一个很宽的峰,这是Ni+ 2和Ni+ 3振荡卫星峰。用氧化镍峰对应的高斯曲线与XPS光谱进行匹配。这些发现与早期对反应磁控溅射制备的氧化镍薄膜中Ni 2p3/2的组成和化学状态的研究一致[47,48,49]。
Ag 3d核能级结合能的窄扫描XPS谱如图2c所示。Ag 3d5/2和Ag 3d 3/2的核能级结合能分别为368.2和374.2 eV[50]。在368.2 eV处的低能峰归因于薄膜中的Ag金属,而在374.2 eV处的低能峰归因于NiO基体中Ni取代位的Ag。在假定银成分在表面区域是均匀的情况下,通过仔细比较光谱中的峰高,就有可能确定近表面区域的成分。XRD分析结果中没有Ag相关相,而XPS观察到表面存在Ag离子,表明Ag离子在NiO基体中被氧化。
图2描述了NiO-Ag薄膜的O1s光电子信号的反褶积。分析NiO-Ag薄膜氧的1s谱线,发现氧原子的存在来自M-O峰(529.6 eV结合能)和OH峰(531.7 eV结合能),而533.3峰是由薄膜表面吸收的水或其他含氧物质如OH或CO引起的。这说明了材料的表面不稳定性是如何随着氧气的存在而增加的。在XPS数据中,OH相的存在程度小于氧态I (O 1s)。x射线衍射(XRD)测量没有揭示这一点。图2e给出了O-C-O含氧碳质带和C-O峰的结合能分别为286.3和288.2 eV。C-C键由结合能为284.6 eV的反卷积峰来识别[51]。根据XPS的研究,所有沉积的薄膜都是单相的NiO-Ag复合材料。
3.3 形态分析
不同沉积时间(200,400,600和800s)的所有NiO-Ag薄膜的FESEM图像如图3所示。图像显示,通过延长沉积时间和显示更多的颗粒团块,膜是如何粗糙的。形貌上晶粒大小不均匀;合成的薄膜也有明显的缺陷。采用能谱仪对沉积膜NiO-Ag-200进行元素分析,如图4d所示;对Ni、O和Ag元素的光谱进行了清晰的观察,证实了沉积的Ni - Ag薄膜的纯度,这一结果与XPS的结果一致。能谱图也证实了FTO衬底表面上不同元素(Ni、O和Ag)的均匀分布,如图4a-c所示。
NiO-Ag薄膜在a200、b400、c600和800s沉积的FESEM图像
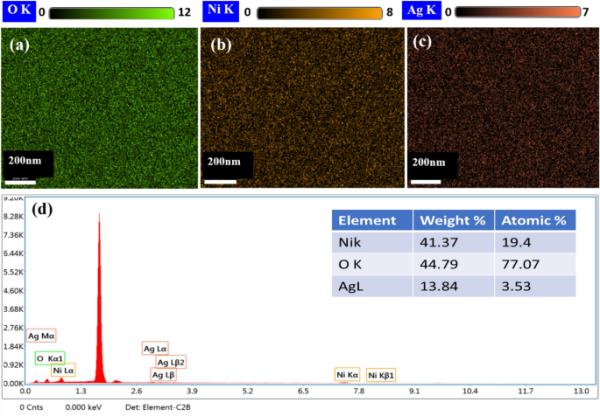
nio - ag200的能谱,a O, b Ni, c Ag和d Ni, O和Ag的元素映射图
扫描电镜图像以45度倾斜拍摄,以确定沉积时间如何影响所得薄膜厚度(见图5)。很明显,在制备过程中延长沉积时间会增加薄膜厚度。NiO-Ag-200薄膜的厚度约为17 nm(图5a),而NiO-Ag-800薄膜的厚度约为100 nm(图5d),增加了5倍。

用FESEM对NiO-Ag的a200、b400、c600、d800进行了薄膜厚度表征
3.4 光学分析
紫外-可见光谱法对透光率的分析如图6所示。随着层厚的增加;透光率有明显的和预期的下降,这可能是由于更简单的电荷转移引起的。利用Tauc关系计算薄膜带隙,如式[52,53,54]所示。
(4)其中A为常数,h为入射光子的能量,(α)为吸光度系数。根据不同材料的量子选择原理,(n)可分别为直接带隙和间接带隙的1/2或2。
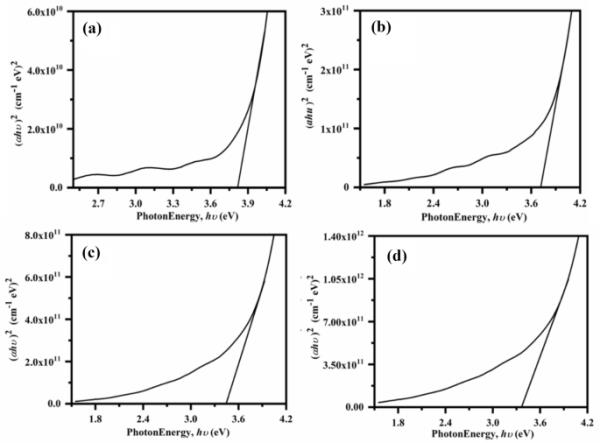
用线性面积与光子能量(hv)轴的交点来评价薄膜的带隙。图7显示了厚度对带隙值的影响;NiO-Ag-800的带隙最小,为3.36 eV,而NiO-Ag-200的带隙最大,为3.81 eV。原因可能与结晶度的增强有关,如上所述的XRD和FESEM;也有研究表明,当薄膜厚度增加时,能带结构中的局域态可能与能带边界重叠,从而使带隙最小化[36,37]。
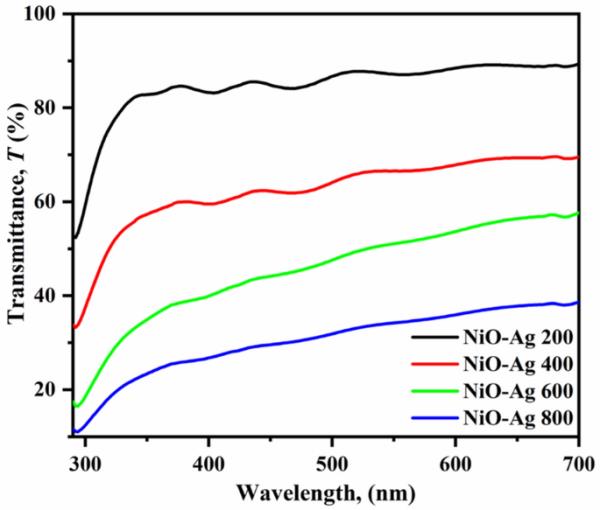
所制备薄膜的光学透过率

所制备薄膜的光学带隙
3.5 Electrocatalytic活动
在0-0.6 V的电位窗口内,在0.5 M KOH电解质中,所有薄膜在不同扫描速率(5、10、20、30、50和100 mv s−1)下与Ag/AgCl的CV曲线如图8所示。在阳极和阴极扫描中,与Ni2+/Ni3+活化相关的是一对峰(氧化和还原)。Ni和Ag提供了两个电活性中心来丰富氧化还原过程,同时改善氧化过程。阳极和阴极电流密度随着沉积时间的增加而增加,这是由于薄膜的厚度增加,其中含有大量的Ni和Ag,增加了活性位点。从扫描电镜图像中可以看出,较厚的样品表面暴露出更多的活性位点,可能有二次电子转移在起作用。
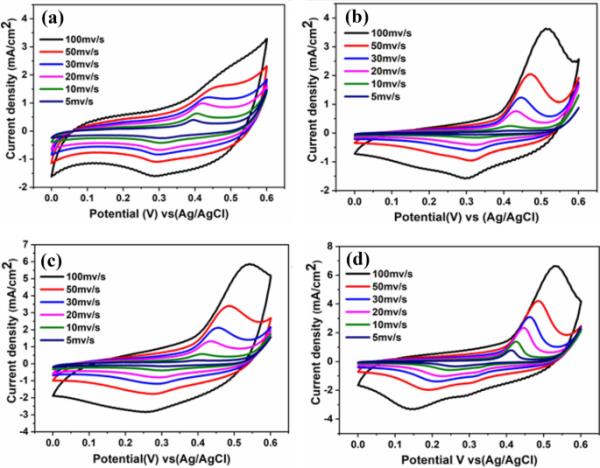
在0.5 M KOH条件下,不同扫描速率下薄膜的循环伏安图:a NiO-Ag-200, b NiO-Ag-400, c NiO-Ag-600, d NiO-Ag-800
图9显示了各膜阳极和阴极电流密度与扫描速率平方根(5-100 mV/s)之间的线性关系。结果表明,扫描速度的增加导致氧化还原反应的增加,并且OH−向孔腔的迁移改善了电化学过程[55]。从图中可以明显看出这一点。(8和9)表明,NiO-Ag-800在各种扫描速率下的氧化还原反应中表现优于其他材料,因为它具有大量的Ni+ 2、Ni+ 3和Ag,由于形成多个连续层以增加厚度,这些元素已经扩散到FTO表面。这通过加速OH -离子在表面的扩散来提高催化活性。
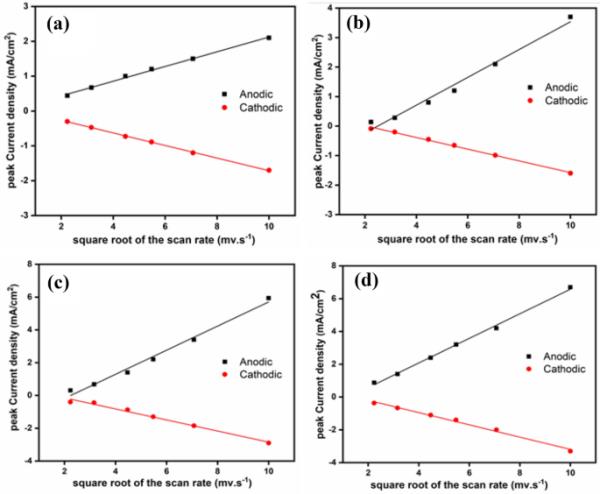
得到了NiO-Ag-200、b NiO-Ag-400、c NiO-Ag-600、d NiO-Ag-800阳极和阴极电流密度与扫描速率平方根的关系
3.6 甲醇氧化的电催化活性
合成的薄膜在0.5 M KOH和0.5 M甲醇混合的碱性电解质中以50 mV s−1扫描速率测试甲醇氧化性能,如图10所示。Ag/AgCl作为参比电极,铂作为反电极。描述任何电催化剂的电化学特性的两个关键变量是电流密度和起始电位。电流密度随着膜厚的增加而增加,NiO-Ag-800 NiO-Ag-600、NiO-Ag-400和NiO-Ag-200分别为10.5、10、9、8 mA cm−2,如图11a所示,其原因是由于沉积时间长,沉积材料量增加,导致Ni和Ag增加,这是机理中报道的甲醇氧化的活性位点[56]。起始电位不变,为0.37 V。这是正常的,因为EDX结果证实元素之间的比率是恒定的。膜具有良好的甲醇氧化活性是由于XRD所示的良好结晶[57]。此外,二维结构(薄膜形状)在暴露大表面和增加薄膜的反应活性面积方面起着重要作用。如果我们将这些结果与之前报道的一些催化剂进行比较,这些结果非常有希望,如表2所示。NiO-Ag-800在不同浓度的甲醇(0.5、1和2 M)下进行了测试,但在0.5 M的甲醇中结果最好,如图11b所示。
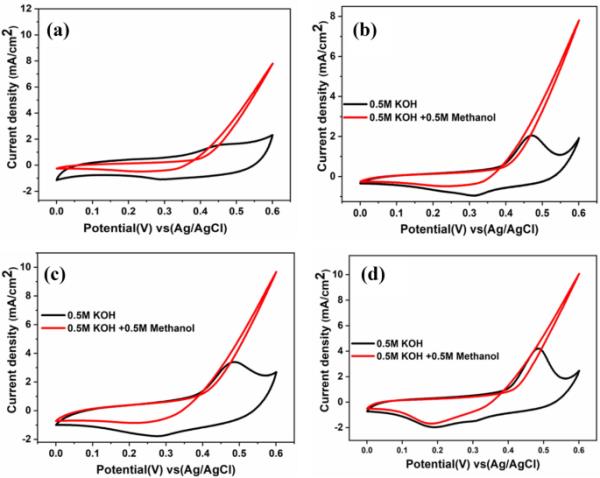
薄膜在0.5 M KOH + 0.5 M甲醇溶液中,扫描速率为50 mV/s,室温下NiO-Ag 200 b NiO-Ag 400 c NiO-Ag 600 d NiO-Ag 800的循环伏安图
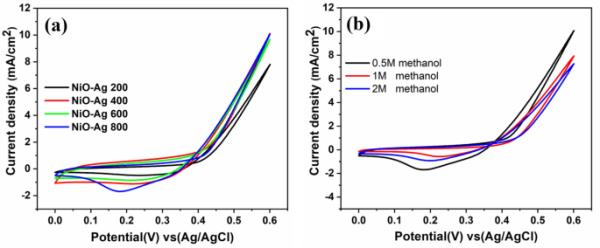
a薄膜在0.5 M KOH + 0.5 M甲醇溶液中以50 mV s−1的扫描速率在室温下的循环伏安图;b不同浓度甲醇在50 mV/s的扫描速率下对Ag-NiO 800的循环伏安图
许多文章描述了NiO氧化甲醇的机理[64,65,66,67]。
(5)或
(6)或
NiO-Ag薄膜通过具有(Ni+ 2和Ni+ 3)氧化还原对和Ag的电催化活性位点吸附电解质介质中的甲醇分子。因此,吸收的MeOH经过电氧化后,CO中间体留在电催化剂表面,然后OH -离子从支撑电解质吸附到NiO膜的捕集中心。最后,CO氧化物通过吸附的OH分子转化为CO2,恢复电活性位点,增强长期稳定性[68]。
图12a显示了频率范围为(0.01至100,000)Hz的电化学阻抗测量,使用面积为1 cm2的薄膜,在0.6 V下vs. Ag/Ag Cl, 0.5 M KOH中含有0.5 M甲醇。根据碱性介质中MOR的机理,可分为以下几个步骤:
(7) (8) (9)其中M作为电极表面的活性位点。
机理从式7中的羟基离子氧化吸附开始。然后通过甲醇的脱氢氧化吸附产生吸附的一氧化碳,如式8所示。因此,式9演示了如何制造二氧化碳并补充活性催化位点。包括电解液的电阻在内,所有薄膜的直径一般都是不超过26欧姆的小半圆。观察到EIS随着FTO上沉积薄膜厚度的增加而降低,因为离子强度增加,导致整个MOR过程中的电荷转移动力学增强。
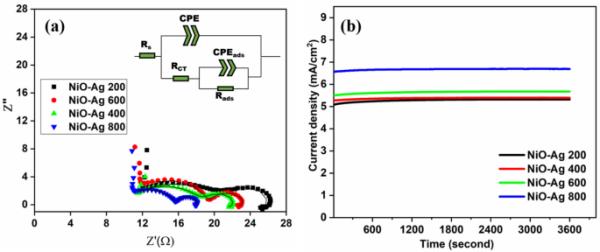
a奈奎斯特氧化反应图,b薄膜稳定性,在0.60 V下,使用0.5 M甲醇
利用图12a所示的等效电路对EIS数据进行拟合。其中Rs为电解液电阻,CPE为恒相元件,Rct为电荷转移电阻。同时,Cads和Rads是与中间反应吸附相关的元素,如表3所示。NiO-Ag膜的Rads很低,表明其甲醇氧化动力学较快,甲醇吸附较简单。
图12b显示了在0.6 V恒定电压下,通过计时安培测试评估的薄膜的长期稳定性活性。可以观察到,在周期时间结束时,初始电流密度值没有衰减,这说明所有电极都具有很强的稳定性。大多数用于甲醇氧化(MOR)的电催化剂,即使是珍贵的和市售的Pt,都不能持久,因为在电极表面会积聚碳质反应中间体,如CO。因此,长期稳定性测试是检验优良电催化剂的重要手段。
4 结论
采用简单的共溅射物理气相沉积方法成功地合成了NiO-Ag薄膜。该方法制备的薄膜具有分散均匀、比表面积高的小晶体等优点,可以很好地作为甲醇氧化电催化剂。因此,经EDS证实,元素在FTO衬底表面的良好分布导致了电活性位点的增加,帮助ag掺杂的NiO作为MOR的有效电催化剂,正如电化学测量所显示的那样,因为反应动力学加速和离子扩散增强。此外,研究结果表明,薄膜的电活性随厚度的增加而增加,其中Ag - nio -800记录的最低起始电位为0.37 V /Ag /AgCl。根据制备方法,所有的Ag-NiO薄膜都表现出良好的稳定性,薄膜生长在金属衬底上,以增加附着力,不添加任何粘合剂或导电剂,直接用作MOR的电催化剂。
下载原文档:https://link.springer.com/content/pdf/10.1007/s10854-023-11029-x.pdf





