摘要
[99mTc]以脑为靶点放射合成氟图西坦评价神经精神疾病。用锝-99m对益智药物进行了标记,并对影响标记收率的因素进行了研究。在最佳条件下,获得了高放射化学产率(98.9%)的放射复合物,并在生理盐水中稳定长达36小时,在血清中稳定超过24小时。标记的氟图西坦肼在硅中进行了表征和评估。在小鼠体内的生物分布研究表明,在注射后5分钟,该复合物的脑吸收量为每克注射剂量的8.8% (% ID/g),超过市售的[99mTc] ECD (4.7% ID/g)和[99mTc] HMPAO (2.25% ID/g)。所有结果表明,示踪剂是一个很好的候选成像人脑评估神经精神疾病。
介绍
人脑是一个复杂的器官。中枢神经系统疾病(如精神疾病和神经退行性疾病)背后的详细分子和亚细胞过程以及神经元细胞相互作用尚不清楚[1,2]。在过去的几十年里,单光子发射计算机断层扫描(SPECT)作为一种临床诊断和研究方式越来越重要[3,4]。SPECT可以通过实时可视化、体内表征和鉴定复杂的生物过程和特定途径,大大增加我们对神经精神疾病发病机制和治疗的理解[1]。这项吸引人的技术为药物开发[5]和评估生化过程[6]提供了有用的工具。
外消旋类分子是以内源性神经肽环丙氨酸为基础的神经保护剂和代谢促进剂[7]。它们主要被用作治疗认知缺陷的益智药物。尽管外消旋胺的确切作用机制尚不完全清楚[8],但人们认为它们主要通过调节α-氨基-3-羟基-5-甲基-4-异恶唑丙酸(AMPA)受体来产生作用[9,10];主要的兴奋性神经递质受体在大脑中介导突触传递。AMPA受体功能障碍被认为是某些神经元疾病的基础,包括抑郁症、精神分裂症、癫痫和阿尔茨海默病[11,12,13],它们的突触运输被认为是神经元可塑性的基础,包括学习和记忆[14,15]。近年来,基于消拉西坦分子的几种示踪剂被开发用于脑成像[16,17,18,19,20,21,22,23]。
氟图西坦肼是一种合成的精神刺激拉西坦分子,其效力比吡拉西坦强30 - 60%,适用于更广泛的适应症[10]。放射性标记的氟图西坦肼可以提供一种可视化人类活体大脑的工具。因此,它可以帮助进一步阐明神经元疾病的分子和电路基础,并有助于开发新的诊断和治疗方案。本研究研究了氟图西坦肼用γ-发射器锝99m进行放射性标记,并初步评价了其作为脑成像示踪剂的潜在用途。
实验
材料
在这项工作中使用的所有化学品和试剂都是最高纯度的。Fonturacetam hydraide, 2-(2-oxo-4- phenylpyrolidin -1-yl)乙酰肼,MW 233.27,购自美国新泽西州ChemScence公司。高技术酸盐从比利时布鲁塞尔ELUTEC公司提供的钼发生器中洗脱。采用双蒸馏氮气净化水进行溶解和稀释。瑞士白化病小鼠(体重20 - 25g)用于生物分布研究,并从埃及原子能管理局标记化合物部动物室获得。采用Vario EL元素分析仪进行元素分析。1H-NMR和13C-NMR谱用Bruker AMX 500 MHz光谱仪在CDCl3 (TMS内标)中进行。质谱采用Agilent Technologies三重四联质谱仪,极性设置为电喷雾电离(ESI)正模式。
方法
标签nturacetam酰肼
将二水氯化亚锡溶液(150µg, 0.2 mL)加入到氟图西坦肼溶液(25µg, 0.5 mL)中,磷酸盐缓冲液(pH 6, 0.1 M)保持在无菌青霉素瓶的正氮压下。之后,将从钼生成器中新洗脱的高技术酸盐溶液(~ 350 MBq)加入到该混合物中,随后在室温下孵育25分钟。为了确定最佳标记条件,在不同pH值(2-11)下,使用不同量的氟图西坦肼(5-50µg)、二水合氯化亚锡(25 - 250µg)、不同反应时间(5-40 min),研究了影响标记收率的不同因素组合。
放射化学纯度分析
采用硅胶浸透薄层色谱法(SG-TLC)测定了[99mTc]氟图西坦肼的放射化学纯度。采用两种不同的显影系统(盐水和乙醇:水:氢氧化铵[2:5:1])来测定标记络合物、游离高技术酸盐和胶体的百分比[24]。取反应液的等分(5 μL)于两条薄层色谱条(每条为14 × 1.5 cm2)上斑点。开发是在充满氮气的密闭罐中进行的,以防止标记的斑点被氧化。开发后,将两张放射性色谱图干燥,切成1厘米的片,并使用伽马闪烁计数器分别计数。放射化学纯度是用下面的公式确定的:
HPLC分析及纯化
高压液相色谱(HPLC)采用美国岛津(Shimadzu)型号,配备LC-9A泵、Rheodyne进样器、UV分光光度计检测器(SPD-6A,岛津,美国)和放射性同位素检测器(Bioscan Inc.,美国)。色谱柱为RP - 18 (250 × 4.6 mm,粒径10µm),流速2.0 mL/min。取样体积为10µL。以乙腈/水/乙酸(20:80:0.1%,v/v)为流动相洗脱,在280 ~ 290 nm范围内进行紫外检测。采用高效液相色谱法对[99mTc]氟图西坦肼进行鉴定,证实放射性标记的氟图西坦肼与非放射性铼标记的氟图西坦肼一致[25]。在这方面,放射性标记配合物的等价物与铼类似物共注射。然后比较了紫外通道(280 ~ 290 nm)和辐射通道中检测到的峰的保留时间。
no .的合成与表征非放射性铼类似物
在类似条件下,用过铼酸钾测定[99mTc]氟图西坦肼的结构,合成了分析性铼标准化合物[26]。简单地说,在无菌青霉素瓶中,将2.5 mg(10.7µmol)氟图西坦肼溶解于10 mL磷酸盐缓冲液(pH 6)中,然后超声5分钟使其完全溶解。将1.1 mg(3.9µmol)高透酸钾和2.6 mg(11.4µmol)二水合氯化亚锡分别溶解在最少量的双蒸馏氮气净化水中。然后,将它们添加到反应瓶中。调节反应介质pH至pH 6,在25℃下孵育25 min,纯化产物(Re-fonturacetam hydraide),高效液相色谱分离。然后用1H-NMR和13C-NMR对其进行了表征。采用ACD/NMR Processor V12软件进行核磁共振数据分析和基于相关性的结构预测[27]。1H NMR (500 MHz, CDCl3)谱在δ ppm处显示出峰值:2.66 (d, 2H)、2.89 (d, 2H)、3.11 (d, 2H)、3.21 (m, 2H)、3.26 (d, 2H)、3.66 (d, 2H)、3.76 (d, 2)、4.59 (s, 2H)、6.49 (s, 2H)、7.23-7.26 (m, 10H)、8.38 (s, 2H)。13C NMR (500 MHz, CDCl3)谱在δ ppm处显示出峰值:35.20 (C7, C24)、40.20 (C11, C28)、46.38 (C13, C30)、52.70 (C8, C25)、69.89 (C14, C31)、126.90 (C5, C22)、127.07 (C1, C3, C18, C20)、129.03 (C4, C6, C21, C23)、141.19 (C2, C19)、173.86 (C10, C27)。质谱[m / z(相对丰度)]:31(0.28),41(0.38),79(0.91),105(0.26),117(0.99),119(0.21),158(0.65),160(0.62),162(0.6),174(0.17),184(0.19),186(0.42),188(0.67),199(0.26),201(0.28),203(0.5),218(1),405(0.24),437(0.16),453(0.98),455(0.48),483(0.35),497(0.21),538(0.31),550(0.18),552(0.35),592(0.26),640(0.36),642(0.43),654(0.32),670(0.24)。[99mTc]氟图西坦肼的化学性质已通过RP-HPLC放射色谱与相应的同系物铼的紫外可见迹相比较确定。
计算机评估
利用iGemdock ver2.1软件进行对接研究,评估[99mTc]氟图西坦肼对AMPA受体的靶向能力[20]。目标蛋白的x射线晶体结构从RSCB蛋白数据库(PDB ID: 3KG2)中导入。利用ChemBio3D ultra软件设计[99mTc]氟图西坦肼的结构,然后利用分子力学的能量最小化方法预测配合物的几何优化三维模型[28]。使用iGemdock在受体结合位点内研究所测标记复合物的最合适结合姿态[29]。通过设定种群规模为800,80代,1溶液,对标记的复合体进行精确对接。然后,选择结合能较低的对接配体位姿,分析其与蛋白质残基的相互作用。
体外放射化学稳定性
在室温下检测[99mTc]氟图西坦肼48 h的稳定性。将配合物(1ml)与生理盐水(2ml)混合,并在1、2、4、6、12、24和48 h提取3份样品(2µL),通过SG-TLC方法进行评估[30]。游离高技术酸盐和胶体的增加(以%计)表明标记的络合物解离。在37°C有血清存在的情况下,还评估了稳定性。0.2 mL配合物与1.8 mL人血清混合,孵育48 h。按不同时间间隔从混合物中取等量(2µL),在SG-TLC上标记,如前所述,用生理盐水和乙醇:水:氢氧化铵[2:5:1]进行示踪。计算体外稳定性(in %)[31,32,33]。
分配系数(P)的测定
分配系数是衡量药物亲脂性的一个指标。标记复分割系数(P)采用我们之前报道的方法,稍作修改[34]。简单地说,将新制备的[99mTc]氟图西坦肼与等体积的正辛醇(有机层)和磷酸盐缓冲液(pH 7.4, 0.025 M,水层)在离心管中混合。将混合物在室温下涡流5分钟,然后在8,000 rpm下离心10分钟。随后,将有机层和水层的样品(100 μL)转移到其他管中,使用井型伽马计数器(Scalar Ratemeter SR7, Nuclear Enterprises Ltd., USA)进行计数。实验进行三次,分区系数值用Log P表示,计算公式如下:
生物分布和清除研究
体内实验研究得到了埃及原子能机构动物伦理委员会的批准。研究的设计和方案遵循了标签化合物部门制定的指导方针。选用体重20 ~ 25 g的瑞士白化病小鼠。将小鼠(每组5只)置于代谢笼中,在规定的时间内自由进食和饮水。小鼠适应环境1周后,经尾静脉给药[99mTc]氟图西坦肼0.2 mL, 3.7 MBq。在注射后(p.i)规定的时间间隔(5、15、30、60和120分钟),用氯胺酮麻醉小鼠,称重,解剖以测定示踪组织分布。采用心脏穿刺法采集血液样本。分离主要器官(肝、脾、肺、肾、胃、心、肠和脑),用生理盐水洗涤两次,称重,并用NaI (Tl) γ射线闪烁计数器计算放射性。将所得结果表示为每g组织注射剂量的摄取百分比(% ID/g±SD),并计算示踪剂的消除速率常数。
阻碍学习
在给药前10 min静脉注射不同剂量的未标记氟图西坦肼(0 ~ 1000 μg)阻断瑞士白化病小鼠脑AMPA受体。示踪剂注射后5分钟测定脑示踪剂摄取百分比(n = 5)。
统计分析
所有数据均以mean±SD表示。采用方差分析(ANOVA)检验,当P < 0.05时,认为统计学差异是可重复的。
目录
摘要 介绍 实验 结果与讨论 结论 参考文献 作者信息 道德声明 搜索 导航 #####结果与讨论
[的制备、质量控制和表征]99米Tc)佛nturacetam酰肼
如图1所示,在氟图西坦肼结构中存在供电子原子,如氧和氮,增强了其与过渡金属锝-99m的标记。
氟图西坦肼的化学结构
在pH为6的条件下,将氟图西坦肼(50µg)与高技术酸盐(~ 350 MBq)在二水合氯化亚锡(150µg, 150µL)存在下混合,反应25 min,得到了一种放射化学产率为98.9±1.1%的[99mTc]氟图西坦肼配合物。
用两种色谱技术(SG-TLC和HPLC)检测标记物的放射化学纯度。在薄层色谱中,以生理盐水为流动相时,[99mttc]氟图西坦肼和胶体(99mTcO2·nH2O)保持在原点附近(Rf = 0-0.1),而自由高技术酸盐(99mTcO4−)则沿溶剂前沿迁移(Rf = 0.8-1)。然而,使用由乙醇:水:氢氧化铵[2:5:1]组成的流动相时,只有胶体(99mTcO2·nH2O)留在原点附近(Rf = 0-0.1),而配合物和游离高技术酸盐则沿溶剂前沿移动(Rf = 0.8-1)。
如图2所示,该配合物的HPLC放射色谱图显示,在1.2和11.2分钟的保留时间下,两个不同的峰分别对应于游离高技术酸盐和[99mTc]氟图西坦肼配合物。保留时间为4.9 min时,在紫外通道上可以检测到未标记的氟图西坦肼峰,这表明形成了单个标记的配合物。
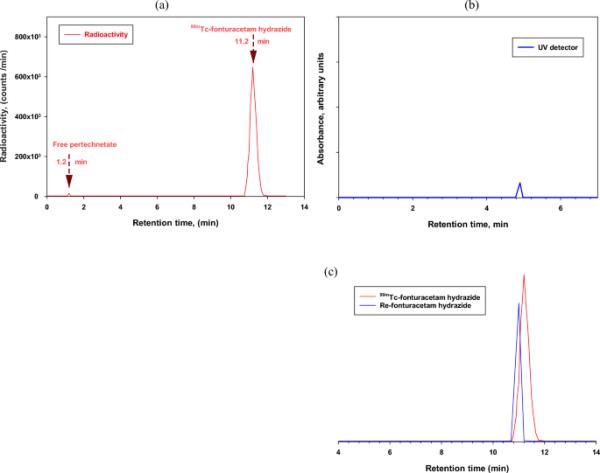
[99mTc]氟图西坦肼配合物(a)和氟图西坦肼配合物(b)的HPLC图谱。放射性示踪剂和相应的铼配合物(c)的对比HPLC图谱。
由于在元素周期表中的位置,锝和铼具有显著的化学相似性。为了阐明锝标记配合物的结构,合成了它的铼类似物并对其进行了表征。使用ACD/NMR Processor V12软件评估核磁共振波谱并将其与结构相关联[29]。[99mTc]氟图西坦肼配合物的结构如图3A所示。使用Chem Draw Ultra 11.0设计标记的复合物结构并进行能量最小化。软件生成优化后的[99mTc]氟图西坦肼配合物三维结构几何图形,理论计算参数值如图3B所示。该配合物预计具有八面体几何结构,配体与金属的比例为2:1。
[99mTc]氟图西坦肼配合物的化学结构。B优化了[99mTc]氟图西坦肼的三维结构
标记反应优化
研究并优化了配体用量、还原剂用量、反应介质pH、反应时间等标记反应参数对[99mTc]氟图西坦肼的最大放射化学产率(RCY)的影响。研究每个因素的实验重复3个重复,结果以mean±SD表示。
配体效应
RCY对氟图西坦肼浓度的依赖性如图4A所示。当氟图西坦肼用量较低时,收率较低(10µg时为46.1±1.6%),主要杂质为胶体形成(~ 12%)。配体浓度不足以使所有还原的锝转化为还原水解的锝胶体[35,36]。当配体浓度为50µg时,反应的最大RCY为98.9±1.1%。再增加氟图西坦肼的用量对RCY没有显著影响,这可能是由于含50 μg的氟图西坦肼溶液以氯化亚锡为还原剂,足以与整个生成的还原剂锝-99m反应。
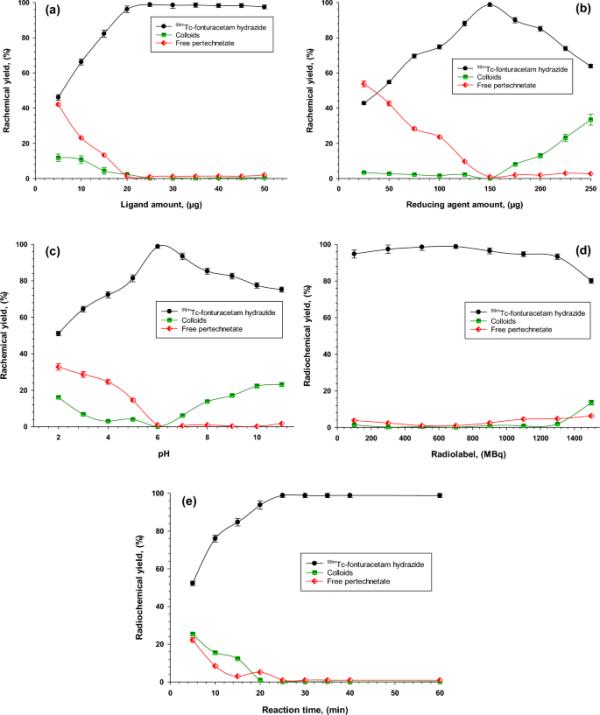
氟图西坦肼、二水合氯化亚锡、pH、高技术酸盐和反应时间对氟图西坦肼配合物放射化学产率的影响
还原剂的作用
二水合氯化亚锡是制备锝-99m放射性药物最常用的还原剂。它降低了从钼发生器洗脱的高氯酸盐离子(+7,放射性标签的来源)到更活泼的低氧化状态。如图4B所示,RCY %取决于反应介质中还原剂的量。在低锡含量(25µg)时,% RCY较低(42.8±0.7%),表明锡不足以还原所有高铁离子。随着SnCl2·2H2O用量的增加,收率逐渐提高,达到最有效浓度(150µg), RCY为98.9±1.1%。进一步增加还原剂浓度,RCY逐渐降低,因为形成了不需要的水解氧化锡胶体[37,38,39]。
pH的影响
反应pH是一个需要控制的关键因素,因为它影响标记过程,并可能影响标记配合物的稳定性。将pH值从高酸性变为高碱性,显著改变了最佳放射化学转化(图4C)。pH值为6,这可能部分反映了[99mTc]氟图西坦肼配合物的稳定性(98.9±1.1%)。pH值为2时,RCY较低(51.1±1.2%),以游离高技术酸盐为主(32.8±1.8%)。当pH值高于最佳值时,RCY在pH值为9和11时分别降低至82.6±1.8和75.2±0.4%,形成的主要物质为氢氧化亚锡胶体[40]。
辐射组效应塔尔
使用可变量的高锝酸盐活性(100-1500 MBq)来确定重构过程中的最佳放射性浓度,评估过量高锝酸盐存在下配合物的稳定性,并评估对多个患者使用同一瓶以降低成像成本的可行性。如图4D所示,本研究结果显示700mbq为最佳剂量。进一步证明,活性在300-900 MBq范围内,配合物对放射性溶解是稳定的。
反应时间
图4E显示了反应时间对[99mTc]氟图西坦肼配合物RCY的影响。在室温下反应进行得很顺利。RCY在10 min内达到76±1.8%,随着时间的增加,在25 min时达到最大值98.9±1.1%,此后RCY在1 h以上保持不变[41]。
物理化学e估值
稳定
研究了[99mTc]氟图西坦肼的保质期,以评估重组后标记药物仍适合人类使用的时间。图5所示的结果表明,锝-99 m标记的氟图西坦肼在环境温度下保持稳定长达40小时,而没有检测到可能导致示踪剂在非靶器官中积累或干扰成像过程的显著副产物。
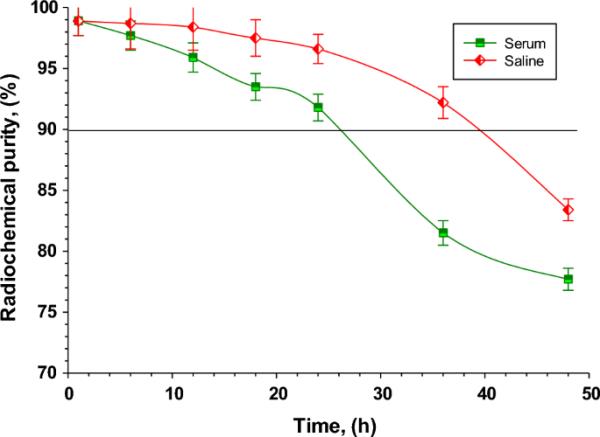
[99mTc]氟图西坦肼配合物在25℃生理盐水和37℃血清中长达48 h的体外稳定性
在血清存在下,在37°C下评估标记复合物的体外稳定性。该复合物在长达24小时内表现出稳定的特征,表明在此期间适合人类给药。之后,48 h内放化学纯度降至77.7±0.9%,可能与血清成分相互作用有关。
分配系数
配分系数是评价候选药物的一个重要标准。它强烈影响药物的药代动力学,如吸收、体内分布以及代谢和排泄的速度。它还通过影响药物在体内到达预定目标的难易程度以及与目标受体的结合强度来控制药理学效果。当血脑屏障的分割系数为1.5 ~ 2.7时,靶向脑的药物穿透血脑屏障的效果最佳。[99mTc]氟图西坦肼实验测定的log P为2.52±0.2。这表明示踪剂的亲脂性及其穿过血脑屏障的能力。
计算机评估
为了评估示踪剂与靶点的结合,使用了iGemdock 2.1软件。该软件创建范德华,氢键和静电相互作用之间的受体和配体的轮廓。然后,它依次读取蛋白质和配体分子原子的目标坐标,并利用柔性对接相互作用分析它们的分子相互作用。然后计算蛋白质活性位点的结合能,以分析蛋白质与配体之间的相互作用。如图6所示,建议的相互作用包括配合物与关键氨基酸(ASN344、GLN337、VAL338和GLU339)之间的氢键和范德华作用。计算机模拟显示,标记的复合物与靶蛋白的配体结合位点具有最佳契合度(能量=−102.05 kcal/mol)[19,20]。
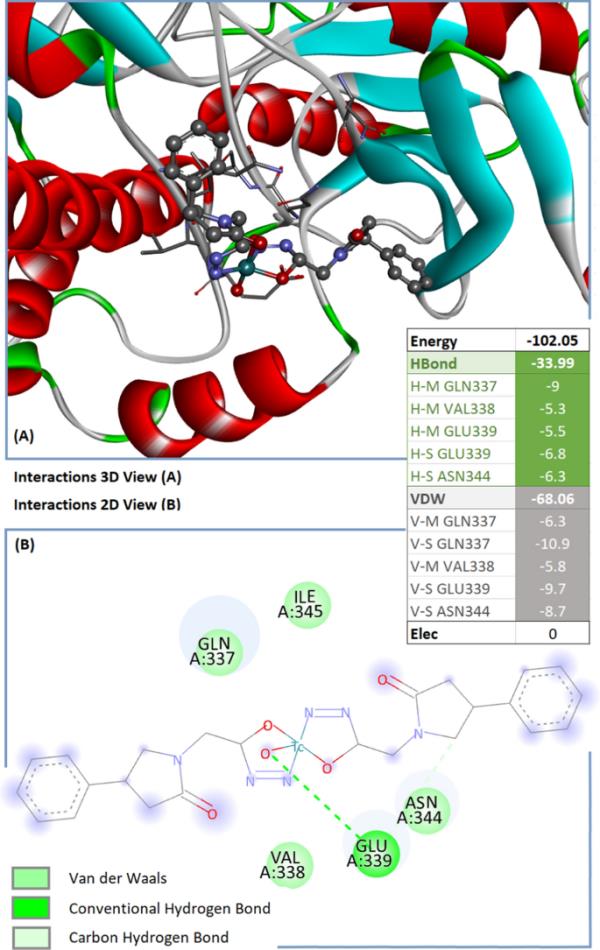
[99mTc]氟图西坦肼与AMPA受体的对接位姿及相互作用谱
生物分布和清除研究
所有生物实验均按照埃及原子能机构动物伦理委员会(伦理批准EAEA/2022/188)制定的指导方针进行。研究了[99mTc]氟图西坦肼在瑞士白化病小鼠体内各器官/组织的摄取情况。收集数据,用5次实验的平均值±SD表示,结果如表1所示。结果显示示踪剂在全身的快速分布。注射后5min血活度较高(22.3±0.5% ID/g), 120min血活度缓慢下降至(6.2±0.2% ID/g),可能与血浆蛋白结合有关。氟图西坦肼由肝脏代谢,这解释了相对较高的肝脏放射性摄取(在30min p.i时10.4±0.7% ID/g)。肾脏是标记药物的主要排泄途径;因此,与其他器官相比,肾脏的放射性随时间增加,达到15.8±0.2% ID/g,并保持较高水平。其余器官的放射量在正常范围内。[99mTc]氟图西坦肼在5min p.i时在脑内高度积聚(8.8±0.1% ID/g)。此后,在15、30、60和120 min时,放射性略有下降,分别为7.4±0.2、5.7±0.2、4.5±0.1和2.4±0.1% ID/g。有趣的是,示踪剂在5 min时的最大脑摄取(5.6±0.2)高于目前使用的脑成像放射性药物,如[99mTc] ECD和[99mTc] HMPAO(分别为4.7和2.25%)[42]。脑/血比结果表明,使用[99mTc]氟图西坦肼作为脑成像放射性示踪剂的最佳时间为15-60分钟。几种标记的外展胺在注射后5分钟小鼠的脑摄取和脑血比如表2所示。
清除研究的结果如图7所示,显示示踪剂遵循一阶消除动力学,其中每单位时间内去除恒定百分比的药物。通过计算得到消去速率常数为0.63 h−1。
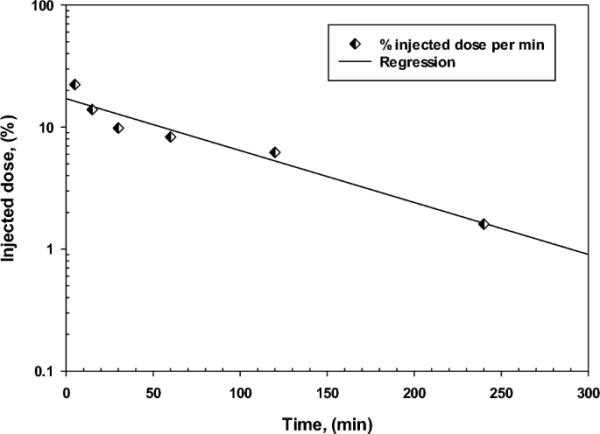
瑞士白化病小鼠对氟图西坦肼[99mTc]的血液清除率
阻碍学习
在示踪剂注射前,用不同剂量的未标记肼氟图西坦(0 ~ 1000 μg)预给药。预给药后,测定每分钟5min氟图西坦肼的脑摄取[99mTc],结果如图8所示。我们观察到,未标记的氟图西坦肼以剂量依赖的方式阻断了大脑对示踪剂的摄取,这表明其积累反映了与蛋白质靶标的相互作用。结果表明,该示踪剂可用于脑成像。
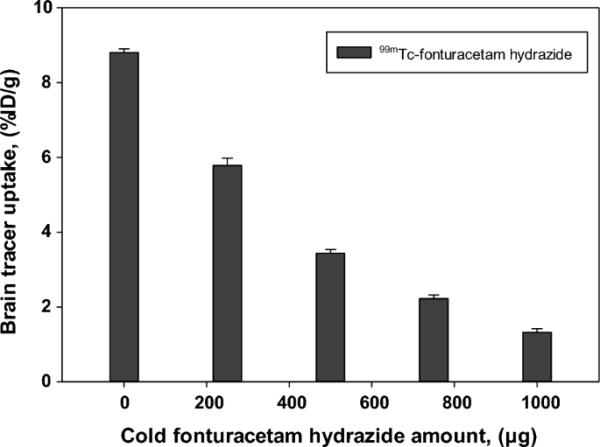
预给药不同剂量未标记肼氟图西坦对正常瑞士白化病患者注射后5min [99mTc]氟图西坦脑摄取的抑制作用
下载原文档:https://link.springer.com/content/pdf/10.1007/s10967-023-08966-6.pdf

